17765 0
טיפול לא תרופתי
ב-AF היא מוגבלת ומסתכמת בהדרה של גורמים המעוררים התקפיות במטופל מסוים (צריכת אלכוהול, פעילות גופנית אינטנסיבית), המלצות תזונתיות סטנדרטיות בחולים עם אי ספיקת לב והשפעות פסיכותרפויטיות.
הקלה של AF paroxysmal
עם הפרוקסיזם הראשון של AF, תמיד צריך לנסות לעצור אותו.
הבחירה בתרופה אנטי-אריתמית להקלה בתרופות של AF התקפי תלויה במידה רבה באופי המחלה הבסיסית, משך קיומו של AF, נוכחות או היעדר סימנים של אי ספיקה חריפה של חדר שמאל ואי ספיקת כלילית. גם להפיכה רפואית של AF paroxysmal תרופות נגד הפרעות קצבעם יעילות מוכחת, השייכת לסוג I (פלקאיניד, פרופנון) או לדרגה III (דופטיליד איבוטיליד, ניבנטן, אמיודרון), או מה שנקרא "פחות יעילות או לא נלמד מספיק" תרופות אנטי-אריתמיות מסוג I (פרוקאיןמין, כינידין). אין להשתמש בגליקוזידים לבביים ובסוטלול כדי לעצור את הצורה ההתקפית של AF.
אם הפרוקסיזם של AF נמשך פחות מ-48 שעות, ההקלה שלו יכולה להתבצע ללא הכנה מלאה של נוגד קרישה, עם זאת, מתן של הפרין לא מפורק 4000-5000 IU תוך ורידי או הפרינים במשקל מולקולרי נמוך (סידן נאדרופרין 0.6 או נתרן אנוקספרין 0.4 שניות / ג) מוצדק.
אם הפרוקסיזם של AF נמשך יותר מ-48 שעות, הסיכון לפתח סיבוכים טרומבואמבוליים עולה באופן דרמטי; במקרה זה, יש להתחיל טיפול נוגד קרישה מלא (warfarin) לפני שקצב הסינוס משוחזר. יחד עם זאת, יש לקחת בחשבון ש-AF יכול להסתיים באופן ספונטני (צורה התקפית) הרבה יותר מוקדם מאשר וורפרין יכול להשיג ערך INR טיפולי של 2.0-3.0. במקרים כאלה, לפני שחזור קצב הסינוס, רצוי ביותר להתחיל טיפול בו-זמני עם וורפרין ו-LMWH (נדרופארין, אנוקספרין במינון של 0.1 מ"ג/ק"ג כל 12 שעות); LMWH מתבטל רק כאשר מגיעים לרמה הטיפולית של INR.
הפרעות המודינמיות חמורות (הלם, קריסה, אנגינה פקטוריס, בצקת ריאות) במהלך הפרוקסיזם של AF מחייבות טיפול מיידי בדחפים חשמליים. במקרה של חוסר סובלנות או חוסר יעילות חוזרת (בהיסטוריה) של תרופות אנטי-ריתמיות, הקלה על הפרוקסיזם מתבצעת גם בעזרת טיפול בדחפים חשמליים.
מתן תוך ורידי ראשון של תרופה נגד הפרעות קצב בחייו של המטופל מתבצע תחת בקרה של ניטור א.ק.ג. אם יש עדויות ליעילות של חומר אנטי-אריתמי כלשהו באנמנזה, זה עדיף.
- פרוקאינאמיד (נובוקאינאמיד) ניתן לווריד בזרם באיטיות במינון של 1000 מ"ג במשך 8-10 דקות (10 מ"ל של תמיסה 10% מדוללת ל-20 מ"ל עם תמיסת נתרן כלוריד איזוטונית) או תוך ורידי בטפטוף (אם יש נטייה ליתר לחץ דם עורקי, בזריקה הראשונה) תחת ניטור מתמיד של לחץ דם, קצב לב וא.ק.ג. בזמן שחזור קצב הסינוס, מתן התרופה מופסק. בקשר לאפשרות של הפחתת לחץ דם, יש לתת אותו במצב אופקי של המטופל, עם מזרק מוכן עם 0.3-0.5 מ"ל של תמיסה 1% של פנילפרין (מזטון) בקרבת מקום. היעילות של פרוקאינאמיד ביחס להקלה ב-AF paroxysmal ב-30-60 הדקות הראשונות לאחר המתן נמוכה יחסית ומסתכמת ב-40-50%. מתן חוזר של התרופה במינון של 500-1000 מ"ג אפשרי רק במסגרת בית חולים. אחת מתופעות הלוואי הנדירות אך העלולות להיות מסכנות חיים של שימוש בפרוקאינאמיד להקלה על AF עשויה להיות הפיכת AF לרפרוף פרוזדורים עם מקדם גבוההולכה לחדרי הלב והתפתחות של קריסה אריתמוגנית. אם עובדה כזו ידועה מההיסטוריה של המטופל, אז לפני תחילת השימוש ב-Novocainamide, מומלץ לתת 2.5-5.0 מ"ג של verapamil (Isoptin) תוך ורידי, לזכור כי זה יכול לגרום גם ליתר לחץ דם עורקי. ל תופעות לוואי procainamide כוללים אפקט אריתמוגני, הפרעות קצב חדריות עקב התארכות מרווח Q-T; האטה של הולכה אנטרו-חדרית, הולכה תוך-חדרית (מופיעים לעתים קרובות יותר בשריר הלב הפגוע, מופיעים ב-ECG כהרחבת קומפלקס החדרים וחסימה של הרגליים של צרור His); תת לחץ דם עורקי (עקב ירידה בעוצמת התכווצויות הלב ואפקט הרחבת כלי הדם); סחרחורת, חולשה, פגיעה בהכרה, דיכאון, דליריום, הזיות; תגובות אלרגיות. התוויות נגד לשימוש של procainamide: תת לחץ דם עורקי, הלם קרדיוגני, CHF; sinoatrial ו-AV block II ו-III דרגה, הפרעות הולכה תוך חדרית; הארכה של מרווח ה-Q-T ואינדיקציות של אפיזודות של טכיקרדיה פירואט בהיסטוריה; מְבוּטָא אי ספיקת כליות; זאבת אדמנתית מערכתית; רגישות יתרלתרופה.
- Nibentan, תרופה אנטי-אריתמית ביתית מסוג III, קיימת רק בצורה של תמיסה. כדי לעצור את הצורה ההתקפית של AF, ניבנטן ניתנת תוך ורידי בטפטוף או סילון באיטיות במינון של 0.125 מ"ג לק"ג (10-15 מ"ג) תחת ניטור א.ק.ג מתמיד, המתבצע לפחות 4-6 שעות לאחר הסוף. של מתן תרופה ומוארך ל-8 שעות אם מתרחש אי ספיקת חדרית.הפרעות קצב. אם הנטילה הראשונה של nibentan לא יעילה, אפשר לתת מחדש את התרופה לאחר 20 דקות באותו תנוחה. היעילות של nibentan במונחים של הפסקת הצורה ההתקפית של AF ב-30-60 הדקות הראשונות לאחר המתן היא כ-80%. מכיוון שסביר שפיתוח של תופעות פרו-קצב רציניות כמו VT פולימורפי מסוג "פירואטה", השימוש בניבנטן אפשרי רק בבתי חולים, בתנאים של יחידות טיפול נמרץ ויחידות טיפול נמרץ לב. אין להשתמש בניבנטן בשלב הטרום-אשפוזי על ידי רופאים של צוותי אמבולנסים ובמרפאות.
- לא ניתן להמליץ על Amiodarone, בהתחשב במוזרויות הפרמקודינמיות שלו, כאמצעי לשיקום מהיר של קצב הסינוס בחולים עם AF התקפי. ההשפעה המקסימלית שלו מתפתחת לאחר 2-6 שעות. על מנת להפסיק את הצורה ההתקפית של AF, אמיודרון ניתנת תחילה כבולוס לווריד בקצב של 5 מ"ג/ק"ג, ולאחר מכן ממשיך להינתן בטפטוף במינון של 50 מ"ג. /h. עם תכנית זו של מתן אמיודרון, קצב הסינוס משוחזר ב-70-80% מהחולים עם AF התקפי במהלך 8-12 השעות הראשונות. מחלות בלוטת התריסאין להפריע למתן יחיד של התרופה.
- Propafenone (ב / בהחדרה של 2 מ"ג / ק"ג למשך 5 דקות, במידת הצורך, החדרה מחדש של מחצית המנה המקורית לאחר 6-8 שעות). במספר מטופלים ללא מחלת לב אורגנית חמורה, ניתן להשתמש בהצלחה בצריכה חד-שלבית של 300-450 מ"ג של פרופנון דרך הפה לטיפול עצמי בפרוקסיזם של AF על בסיס אמבולטורי (עקרון "הגלולה בכיס"). עם זאת, לפני שממליצים למטופל על שיטה זו לחסל AF, יש לבדוק שוב ושוב את יעילותה ובטיחותה (היעדר הפרעות קצב חדריות, הפסקות וברדיקרדיה לאחר נטילת פרופאנון) במצבים נייחים.
- Quinidine 0.2 (צורה ממושכת) 1 טבליה אחת ל-6-8 שעות, בכמות של לא יותר מ-0.6 ליום.
- איבוטיליד (מתן IV של 1 מ"ג במשך 10 דקות, במידת הצורך - מתן חוזר של אותה מנה), או דופטיליד (125-500 מ"ג דרך הפה בהתאם לרמת הסינון הגלומרולרי), או פלקאיניד (מתן IV של 1.5-3.0 מ"ג / ק"ג למשך 10-20 דקות או בליעה במינון של 300 מ"ג); כל שלוש התרופות עדיין אינן זמינות ברוסיה.
צורה התקפית של פרפור פרוזדורים
מבוא
טיפול בהפרעות קצב לב הוא אחד הנושאים הבעייתיים של הקרדיולוגיה עקב היעדר גישה אחידה לטיפול בהפרעות קצב לב, כמו גם ביטוי של השפעה פרו-קצבית בתרופות האנטי-אריתמיות עצמן / AARP / - בממוצע עד 10 % מהמקרים. לא כל סוגי הפרעות קצב דורשים טיפול חירום; במקביל, יש צורך לעבור בזמן שיטות שמרניותטיפול עד ניתוח. AF היא אחת מהפרעות קצב הלב החמורות והשכיחות ביותר. שכיחות AF באוכלוסייה הכללית היא 0.4% (קושאקובסקי מ.ס. פרפור פרוזדורים. גורמים, מנגנונים, צורות קליניות, טיפול ומניעה. סנט פטרסבורג. פוֹלִיוֹ. 1999. 176), מעל גיל 60 - ב-5% מהאוכלוסייה, בקרב אנשים מעל גיל 75 - ב-14%. AF מדורגת במקום השני, אחרי extrasystoles, מבחינת השכיחות בקרב הפרעות קצב. בצפון אמריקה רשומים 2.2 מיליון חולים עם AF, באירופה - 4.5 מיליון. בגרמניה לבדה סובלים ממנה כמעט מיליון אנשים. עלות הטיפול בחולים עם AF במדינות האיחוד האירופי היא 13.5 מיליארד יורו בשנה (ACC/AHA/ESC). AF התקפי מהווה יותר מ-40% מכלל המקרים של AF. עם זאת, בהינתן האפשרות של התקפיות אסימפטומטית, נראה כי השכיחות של צורה זו של AF היא הרבה יותר גבוהה. אבחון AF, החולה עלול לא להרגיש או להרגיש כמו פעימות לב. הדופק אינו סדיר בהפרעות קצב. הצליל של הצלילים ניתן לשינוי. גם מילוי הדופק משתנה וחלק מהתכווצויות הלב, במיוחד לאחר הפסקות דיאסטוליות קצרות, אינו נותן גל דופק. בתנאים אלו, ניתן לקבוע את קצב הלב האמיתי רק באמצעות צלילי לב, בעוד שהתדירות הנקבעת על ידי מישוש הדופק נמוכה יותר (חסר דופק). פעילות גופנית מגבירה את תדירות התכווצויות החדרים ואת אי הסדירות שלהם. תסמינים אלה מרמזים על AF. פרפור פרוזדורים ארוך טווח עלול להוביל להתרחבות פרוזדורים מסוימת, אשר ניתן לזהות במחקרים רדיוגרפיים או אקו-קרדיוגרפיים. ב-ECG, גל P נעדר, הדיאסטולה מלאה בתצורה ובקצב לא סדיר של גלים קטנים, המורגשים יותר בעופרת V 1. התדירות שלהם היא 300 - 600 לדקה (בדרך כלל זה לא סופר). קומפלקסים חדריים עוקבים בקצב הלא נכון, הם בדרך כלל אינם מעוותים. עם קצב חדרי שינה תכופים מאוד (יותר מ-150 פעימות לדקה), תיתכן חסימה של רגל ה-PG, בדרך כלל הימנית, של הצרור האטריו-חדרי. בהשפעת הטיפול, כמו גם בנוכחות הפרעות הולכה אטריונוטריקולרית יחד עם AF, התדירות של קצב החדר עשויה להיות נמוכה יותר. בתדירות של פחות מ-60 פעימות לדקה, הם מדברים על צורה ברדיסיסטולית של AF. מדי פעם, יש שילוב של AF עם חסימה אטריווצנטרית מלאה. יחד עם זאת, קצב החדר נדיר וקבוע. באנשים עם PFFP, כאשר רושמים אק"ג מחוץ לפרוקסיזם, במיוחד זמן קצר לאחריו, מתגלה לעתים קרובות עיוות בולט פחות או יותר של גל P. 3. אטיולוגיה של PFFP.
2. יתר לחץ דם עורקיכל בראשית.
3. מומי לב מולדים ונרכשים.
4. קרדיומיופתיה.
5. עמילואידוזיס.
6. המוכרומטוזיס.
7. פריקרדיטיס.
8. אנדוקרדיטיס זיהומית.
9. תירוטוקסיקוזיס.
10. ניוון שריר הלב אלכוהולי.
11. ניוון שריר הלב אחר - דיס-הורמונלי, הקרנות וכו'.
12. צניחת שסתום מיטרלי.
13. Cor pulmonale כרוני.
14. גידול של הלב (מיקסומה, אנגיוסרקומה)
15. גורמים חולפים: אנמיה, היפוקלמיה, תסחיף ריאתי.
16. חולה אחרי פעולות פתוחותעל הלב.
17. ספורטאים.
18. תסמונת P. Brugada.
19. צורה משפחתית של AF הנגרמת על ידי פגם בגן חלבון תעלת יון (אשלגן) הממוקם על כרומוזום 10q.
20. בהיעדר סיבות - AF "אידיופטי".
21. מ"אידיופטי" יש צורך להפריד בין צורות AF שיש להן מצע, מאובחנים על ידי EPS וניתנים לריפוי מלא על ידי אבלציה בתדר רדיו של הסובסטרט בפרוזדורים:
אם יש מסלול נוסף; יוצא מהפה של הוורידים החלולים (מה שנקרא "מוקד" או "חוץ רחמי"). AF הוא סיבוך שכיח של מחלת לב מיטרלי, קרדיווסקלרוזיס טרשת עורקים, קרדיומיופתיה. גורמים חריפים (הפיכים) ל-AF: ניתוח (במיוחד בלב או בחזה), הלם חשמלי, אוטם שריר הלב חריף, דלקת שריר הלב, מחלת ריאות חריפה, PE. בחולים עם AMI, נמצא קשר פרופורציונלי ישיר בין עלייה בחלבון C-reactive לבין AF שאובחן לאחרונה ( קשר של חלבון C-reactive ופרפור פרוזדורים חדש בחולים עם אוטם שריר הלב חריף. Am J Cardiol 2007; 100(5):753-7.) AF נצפה גם בנזק חודרני לשריר הלב כחלק מעמילואידוזיס, המוכרומטוזיס וגם בגידולי לב. ב-AF שאובחן לאחרונה, יש לשלול תירוטוקסיקוזיס או תפקוד לקוי אחר של בלוטת התריס. נדונים גם גורמים נוספים - צניחת מסתם מיטרלי עם רגורגיטציה מיטראלית, הסתיידות של הטבעת המיטרלית והגדלה אידיופטית של פרוזדור ימין. בחלק מהחולים, במיוחד גיל צעיר, AF עשוי להיות קשור לנוכחות של התקפי אחר טכיקרדיה חדרית, במיוחד לעתים קרובות בנוכחות תסמונת עירור מוקדםחדרים (SVC). טיפול מוצלח במחלה הבסיסית יכול לחסל AF. גורם סיכון נוסף הממריץ התפתחות של הפרעות קצב הוא צריכת אלכוהול. ידועה מה שנקרא "תסמונת לב-חג", המאופיינת בהופעת הפרעות קצב לבבשתיינים ללא קרדיומיופתיה מאומתת לאחר צריכת אלכוהול מסיבית, למשל, בהזדמנויות שונות בסוף השבוע. בין המצבים התורמים לחזרה של פרפור פרוזדורים בחולים עם מחלת לב אלכוהולית, יש לציין: הרחבת פרוזדורים, קיצור התקופה הרפרקטורית, האטה בהולכה פרוזדורית, פגיעות מוגברת לאקסטראסטימולים, הופעת פיצול מקוטע. פעילות חשמלית, במיוחד פוטנציאל פרוזדורי מאוחר על א.ק.ג ברזולוציה גבוהה, כמו גם השפעות נוירו-וגטטיביות על הלב, היפוקלמיה ומגנזמיה. בְּ מקרים נדיריםיש AF נוירוגני הנגרם על ידי השפעות נרתיקיות או סימפטיות. זיהוי מנגנון כזה להופעת AF מאפשר לרופא לבחור חומר תרופתי שסביר יותר למנוע את הישנות הפרעת הקצב. נודע כי מוטציות בכרומוזום 10 (g22-24), כמו גם פולימורפיזם גנטי של קולטנים אלפא ובטא אדרנרגיים, מובילים להופעת מקרים משפחתיים של AF. זה הוכח לראשונה על ידי P. Brugada וחב' (1997), שתיאר שלוש משפחות. 21 מתוך 49 קרובי משפחה היו עם AF, שניים מהם נפטרו בגיל 2 ו-46 מ. הפרה חריפה מחזור הדם במוח. לפיכך, בהתבסס על תוצאות המחקרים הנ"ל, ניתן לטעון כי ל-AF עשויה להיות נטייה גנטית.
ב-30% מהמקרים, AF מתרחשת ללא מחלת לב קודמת. 4. פתוגנזה של PFFP.
1. הופעת מוקדים מרובים של אוטומטיזם חוץ רחמי בפרוזדורים.
2. תפקוד לקוי של צומת הסינוס.
3. קיומם של מסלולים נוספים /תסמונת WPW/.
4. היפרטרופיה ועומס יתר LP.
5. שינוי מצב תפקודי NS מרכזי ואוטונומי.
טבלה 1. גורמים אנטומיים ואלקטרופיזיולוגיים התורמים להופעת ו/או תחזוקה של AF
כאשר אדם נסער או מתאמן, קצב הלב עולה וזה נורמלי. אבל יש מצב אחר - כשלים בקצב מתרחשים בצורה כאוטית ללא סיבה. בדרך זו יכולות להתבטא מחלות שונות הנושאות סכנה. אחד מהם הוא הצורה ההתקפית של פרפור פרוזדורים. הערמומיות טמונה בעובדה שזרימת הדם מופרעת בגוף, לא כל חדרי הלב מתפקדים - התקף יכול להסתיים מעצמו, או שהוא יכול להוביל למוות.
כל מגוון פרפור פרוזדוריםהוא כיווץ כאוטי ולא יציב של הלב. בדרך כלל קצב הלב צריך להיות כ-60-80 פעימות לדקה, בזמן מחלה הקצב עולה ל-400-600 פעימות. במקרה זה, הדחפים אינם משפיעים על כל סיבי השריר, וזו הסיבה שהעבודה של חדרי הלב מופרעת. ישנם שני סוגים של מחלה: קבוע ומשתנה.
פרפור פרוזדורים התקפי הוא הסוג הנפוץ ביותר של פתולוגיה, המאופיין בטבע משתנה. התקפים אינם נמשכים כל הזמן, נמשכים בין כמה שניות לשבוע, אך אם לאחר זמן זה המחלה לא נסוגה, אז החולה כבר מתמודד עם צורה קבועה או כרונית.
הסכנה של המחלה היא הפרה של זרימת הדם, הסיכון לקרישי דם עולה, אדם עלול לחוות שבץ איסכמי.
ICD 10 (International Classification of Diseases) מגדיר את קוד I48.0 לפתולוגיה, בדומה לצורות אחרות של מחלה זו.
העובדה היא כי פרפור פרוזדורים התקפי הוא השלב הראשוני של הפתולוגיה. אם לא מטפלים, מתעלמים מהתקפים נדירים שחולפים מעצמם, קיימת סבירות גבוהה להישנות מתמשכת - המחלה תהפוך לכרונית. זכרו שככל שההתקף נמשך זמן רב יותר, כך גדלה הסכנה שהוא נושא – לא רק הלב, אלא כל הגוף אינו מקבל מספיק חמצן וחומרי תזונה. תאים מתחילים למות, ובקרוב יופיעו סיבוכים רציניים.
סיווג פתולוגיה
לדברי הרופאים, פרפור התקפיפרפור פרוזדורים יכול להתבטא בשתי צורות:
- הבהוב - בתמונות א.ק.ג יופיעו התכווצויות תכופות, אך הדחפים יהיו חסרי משמעות בשל העובדה שלא כל הסיבים מתכווצים. התדר עולה על 300 פעימות לדקה;
- רפרוף - צומת הסינוס מפסיק לעבוד, הפרוזדורים מתכווצים בתדירות של עד 300 פעימות לדקה.
ללא קשר לצורה, המחלה נושאת סכנה, שכן מספר לא מספיק של דחפים נכנסים לחדרים. בהתאם לכך, במקרה הכי פסימי הדבר יוביל לדום לב ולמוות של החולה.
סיווג זה אינו לוקח בחשבון את תדירות ההתקפים, ולכן יש סוג אחר של פתולוגיה - חוזרת. זהו שמו של הפרוקסיזם של פרפור פרוזדורים, שחוזר על עצמו עם הזמן. בתחילה, התקפים עשויים להיות נדירים, למעשה אינם מפריעים לאדם, משך הזמן שלהם יהיה רק כמה שניות או דקות. עם הזמן, התדירות תגדל, מה שישפיע לרעה על הבריאות - החדרים יחוו הרעבה יותר ויותר.
מדוע מתפתח הפרוקסיזם?
ברוב המקרים, התפתחות המחלה מקודמת על ידי הפרעות ראשוניות בעבודת הלב. כלומר, מטופלים שאובחנו עם הפרוקסיזם של פרפור פרוזדורים כבר היו רשומים אצל קרדיולוג, שכן היו להם מחלות מולדות או נרכשות.
הסיבות הנפוצות ביותר כוללות:
- תהליכים דלקתיים שהובילו לסטיות בעבודה של מערכת הלב וכלי הדם;
- שבץ איסכמי;
- מומי לב שגרמו להגדלת גודלם של חדרי הלב;
- לחץ דם גבוה, שתרם לעלייה במשקל הלב;
- קרדיומיופתיה מולדת, תורשתית.
עם זאת, הפרוקסיזם יכול להיגרם לא רק ממחלה, אלא גם מאורח החיים השגוי של החולה או מסיבות אחרות. לדוגמה:
- שימוש לרעה באלכוהול ובקפה;
- זיהומים לא מטופלים או שיכרון הגוף;
- חוסר במגנזיום ואשלגן;
- מצב לאחר הניתוח;
- הפרות בעבודת הריאות, שהובילו ללחץ על שריר הלב;
- הפרעות הורמונליות בגוף;
- עומס יתר תכוף ואינטנסיבי, חוסר שינה, דיכאון, דיאטה קפדניתותשישות הגוף;
- שימוש תכוף במשקאות אנרגיה, גליקוזידים וחומרים נוספים המשפיעים על רמת שחרור האדרנלין ותפקוד הלב.
לפעמים אי אפשר לקבוע במדויק את הגורם למחלה, קשה במיוחד לזהות את המקור העיקרי אצל צעירים או מתבגרים.
פתולוגיה יכולה להיגרם על ידי מחלת עורקים כליליים, הפרעות מולדות או נרכשות, כמו גם גורמים אחרים שאינם לבביים. חשוב מאוד לזהות את הסיבה ולחסל אותה, כי בלי זה אי אפשר לדבר על טיפול מוצלח.
כיצד מתבטאת המחלה?

הצורה ההתקפית של פרפור פרוזדורים יכולה להתרחש ללא תסמינים עבור אדם, או שהם יהיו כמעט בלתי נראים, כך שהמטופל לא יבגוד בהפרות החשיבות. חומרת הביטויים תלויה גם בתדירות התכווצות הפרוזדורים, והדחפים נכנסים ללב. התסמינים הרגילים הם:
- פעימות הלב מואצות ללא סיבה נראית לעין;
- ניכרות הפרעות בעבודת הלב - תדירות הצירים אינה יציבה;
- הדופק אינו אחיד, מה שניתן לראות בחיטוט פשוט בבית;
- יש קוצר נשימה גם במאמץ מינימלי או בלעדיו;
- לאדם אין מספיק אוויר, הוא לא יכול לנשום עמוק, במיוחד במצב אופקי;
- כאב באזור הלב;
- חולשה, אובדן כוח כללי וסחרחורת, אפילו אובדן הכרה אפשרי;
- הזעה מוגברת;
- תחושות של פחד בלתי סביר.
למעשה, סימנים כאלה עשויים להצביע על שורה של הפרעות אחרות בעבודת הלב, כך שאי אפשר לקבוע בבית שבאמת יש לאדם התקדמות של פרפור פרוזדורים. זה צריך להיעשות רק על ידי קרדיולוג בהתבסס על נהלי אבחון.
כיצד מתבצעת האבחנה?

לקביעת האבחנה נדרשת בדיקה ראשונית על ידי מטפל ולאחר מכן על ידי קרדיולוג. בקבלה משתמשים במספר שיטות:
- תשאול ובדיקה חזותית - הרופא מקשיב לדופק, מזהה תסמינים וסימנים ויכול לבצע אבחנה מקדימה;
- רנטגן - מאפשר לך לזהות עלייה סבירה בחדרי הלב;
- אלקטרוקרדיוגרמה היא שיטת האבחון המדויקת והנפוצה ביותר. ב-ECG, ניתן לראות היעדר שיניים גדולות, גבהי גלים שונים ואקראיות של התכווצויות שרירים;
- אולטרסאונד היא שיטה שבה רופאים קובעים לא כל כך את הפתולוגיה עצמה, אלא את הסיבות שעוררו אותה;
- אולטרסאונד טרנס-ושט - שיטה זו מאפשרת לקבוע נוכחות או היעדר קרישי דם, דבר שחשוב במיוחד בעת מתן מרשם לטיפול.
אם החולה מניח אילו גורמים עלולים לעורר את המחלה, למשל, צריכת קפה או הפרעות מולדות, יש לדווח על כך למומחה.
הרפואה המודרנית מאפשרת לך לאבחן במהירות ובדייקנות את המטופל. אם לא תדחו ביקור אצל קרדיולוג, ניתן יהיה לזהות הפרות כבר בשלבים המוקדמים, מה שיקל מאוד על הטיפול ויחסל סיבוכים. למשל, מהלם, בצקת ריאות, דום לב או אוטם שריר הלב.
כיצד מטפלים בפרוקסיזם?
פרפור פרוזדורים התקפי אינו משפט, הטיפול מתבצע בהצלחה רבה, ללא קשר לצורה, קצב הלב ומשך ההתקף. ישנן מספר שיטות המאפשרות לך לנרמל את עבודת הלב.
שיטה שמרנית

שיטת הטיפול הקלאסית והפופולרית היא נטילת תרופות שנקבעו על ידי רופא. המטופל נוטל תרופות, מבקר באופן קבוע אצל מומחה לאבחון, מציין שיפור או הידרדרות במצבו. כאן, התבוננות חשובה מאוד כדי שהמחלה לא תתפתח לצורות מסוכנות יותר, ולא תוביל לסיבוכים רציניים. תרופות מסורתיות משמשות לטיפול, כמו לצורות אחרות של פרפור פרוזדורים:
- קורדרון - זמין בצורת תמיסה וטבליות, מפחית את רגישות מערכת העצבים הסימפתטית, בעל השפעה חוסמת, מפחית לחץ ומעכב את הקולטנים של מערכת כלי הדם. התרופה אינה משמשת לברדיקרדיה, עלולה לגרום לפגיעה בזיכרון, ליקוי ראייה, דיכאון ועייפות;
- נובוקאנימד - מעכב את פעילותם של מוקדי עירור של דחפים, מפחית את מוליכות סיבי השריר, מרחיב את כלי המוח. זמין בצורה של טבליות ותמיסה. עלול לגרום לאנמיה, הפרעות בתפקוד מערכת העצבים ואיברי העיכול;
- דיגוקסין הוא גליקוזיד לבבי בעל השפעה חיובית המפחיתה את דרישת החמצן של תאי הלב. זה מאט את הפעילות של הצומת הסינוטריאלי, משפר את תפקוד עצב הוואגוס. התרופה אינה גורמת כמעט לתופעות לוואי שאינן לבביות, למעט כאבי ראש וסחרחורת.
שחזור רפואי של קצב הסינוס ללא טיפול נוסף עם משך התקף של יותר מיומיים טומן בחובו השלכות חמורות, כולל שבץ וחסימת כלי דם.
תרופות אלו או האנלוגים שלהן מתאימות להפסקת התקף וטיפול נוסף, אך יש ליטול אותן רק באישור מומחים. אסור ליטול כדורים לוויסות דופק בעצמך.
שיטות אלקטרופולס

דרך נוספת לטפל במחלה היא ביצוע טיפול בדחפים. שיטה זו משמשת אם למטופל כבר יש סיבוכים, או שהתרופה לא נתנה את התוצאה הרצויה. ההליך מתבצע על פי התוכנית הבאה:
- נעשה שימוש בהרדמה כללית;
- אלקטרודות מוחלות - אחת מתחת לעצם הבריח, השנייה באזור הלב;
- קצב הלב נקבע, המכשיר מסונכרן כך שהפולסים תואמים את הפעימות;
- הערך הנוכחי הרצוי מוגדר;
- מתבצעת פריקה;
- הלב מתחיל מחדש ונכנס לקצב סינוס.
ולמרות שתיאור השיטה מפחיד חולים רבים, בדומה להחייאה של האיבר הראשי, יעילות הטיפול נוטה להיות 100% - כמעט כל החולים מחלימים.
שיטות כירורגיות
אם שיטות טיפול תרופתיות ואלקטרופולס לא הניבו את התוצאה הרצויה, או שהמחלה נוטה להישנות בתדירות גבוהה, מתבצעת התערבות כירורגית - שיטה קיצונית ומסובכת למדי. זה מורכב בהסרת מוקדים פתולוגיים בלייזר. ישנם מספר סוגי פעולה:
- עם פתיחת בית החזה - שיטה מסורתית המשמשת רופאים רבים כבר עשרות שנים. דורש תקופת החלמה ארוכה;
- ללא פתיחת בית החזה - הניתוח מתבצע באמצעות ניקור, נעשה במכשור חדיש בכל מרכזי הקרדיולוגיה. סוג ההתערבות המתקדם והבטוח ביותר;
- התקנת cardioverter - המכשיר אינו פועל כל הזמן, אלא נדלק רק כאשר יש תקלה בלב. פעולה כזו היא די יקרה, המחירים מתחילים ב-2,000 דולר.
טיפול כירורגי משמש רק אם שיטות אחרות חסרות אונים, או שהמחלה מתקדמת, מעוררת התפתחות של סיבוכים באיברים אחרים.
פרפור פרוזדורים התקפי הוא פתולוגיה מסוכנת שעלולה להוביל לתוצאות חמורות. למרבה המזל, כיום מחלה זו מאובחנת במהירות ומטופלת בהצלחה, אך הערמומיות טמונה גם בעובדה שעבור חולה, הפרות יכולות להתרחש ללא תסמינים. כלומר, הפתולוגיה מתפתחת, ו טיפול בזמןלא נרשמים, אז כדאי לבקר רופא באופן קבוע ולעשות א.ק.ג. כדי להבחין בהפרעות בשלבים המוקדמים.
תאריך פרסום המאמר: 13/11/2016
תאריך עדכון המאמר: 06.12.2018
פרפור פרוזדורים (בקיצור AF) הוא הסוג הנפוץ ביותר של הפרעת קצב מבין כל הפרעות קצב הלב.
לעבודה נכונה ויעילה של הלב, הקצב נקבע על ידי צומת הסינוס. זהו האזור שממנו יוצא בדרך כלל האות ללב להתכווץ (כלומר, מתרחש דחף). בפרפור פרוזדורים, התכווצויות (לא דחפים) הן כאוטיות ומגיעות מחלקים שונים של הפרוזדור. תדירות ההתכווצויות הללו יכולה להגיע לכמה מאות בדקה. התדירות הרגילה של התכווצויות היא 70 עד 85 פעימות לדקה. כאשר דחפים עוברים לחדרי הלב, גם תדירות ההתכווצות שלהם עולה, מה שגורם הידרדרות חדהמדינות.
ערכת הולכת דופק

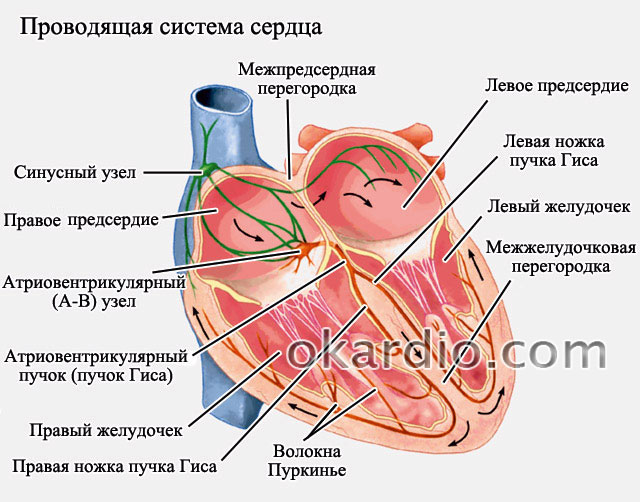
כאשר קצב הלב גבוה (מעל 85 פעימות לדקה), אז מדברים על הצורה הטכיסיסטולית של פרפור פרוזדורים. אם התדירות נמוכה (מתחת ל-65 - 70 פעימות לדקה), אז הם מדברים על צורה ברדיסיסטולית. בדרך כלל, קצב הלב צריך להיות 70-85 פעימות לדקה - במצב זה מדברים על צורה נורמוזיסטולית של פרפור.
גברים חולים לעתים קרובות יותר מנשים. הסיכון לפתח AF עולה עם הגיל. בגיל 60 בעיה זו נמצאת ב-0.5% מכלל הפונים לרופא, ולאחר גיל 75 מתגלה הפרעת קצב אצל כל אדם עשירי.
מחלה זו מטופלת על ידי קרדיולוג, כירורג לב או הפרעת קצב.
על פי הנתונים הרשמיים המוצגים בהמלצות של קרדיולוגים רוסים משנת 2012, פרפור פרוזדורים ופרפור פרוזדורים הם מושגים זהים.
מדוע פרפור מסוכן?
כאשר הצירים כאוטיים, הדם נשאר בפרוזדורים זמן רב יותר. זה מוביל להיווצרות של קרישי דם.
דברים גדולים יוצאים מהלב כלי דם, המובילים דם למוח, לריאות ולכל האיברים הפנימיים.
- טרומבים שנוצרו באטריום הימני דרך גזע ריאתי גדול נכנסים לריאות ומובילים לתסחיף ריאתי.
- אם נוצרו קרישי דם באטריום השמאלי, אז עם זרימת הדם דרך כלי קשת אבי העורקים הם נכנסים למוח. זה מוביל להתפתחות של שבץ מוחי.
- חולים עם פרפור פרוזדורים נמצאים בסיכון לפתח שבץ מוחי(תאונה מוחית חריפה) גבוהה פי 6 מאשר ללא הפרעות קצב.
 היווצרות פקקת באטריום השמאלי מובילה לשבץ מוחי
היווצרות פקקת באטריום השמאלי מובילה לשבץ מוחי גורמים לפתולוגיה
הסיבות מחולקות בדרך כלל לשתי קבוצות גדולות:
שֶׁל הַלֵב.
ללא לב.
לעתים רחוקות, עם נטייה גנטית וחריגות בהתפתחות מערכת ההולכה של הלב, פתולוגיה זו יכולה להיות מחלה עצמאית. ב-99% מהמקרים פרפור פרוזדורים אינו מחלה או סימפטום עצמאיים, אלא מתרחש על רקע הפתולוגיה הבסיסית.
1. סיבות לבביות
הטבלה מראה באיזו תדירות מחלת לב מתרחשת בחולים עם AF:
בין כל הפגמים, פרפור פרוזדורים מזוהה לעתים קרובות יותר עם מומי לב מיטרלי או רב מסתיים. המסתם המיטרלי הוא המסתם המחבר בין הפרוזדור השמאלי לחדר השמאלי. פגמים רב-סתמיים הם התבוסה של מספר מסתמים: מיטרלי ו(או) אבי העורקים ו(או) תלת-צמידי.
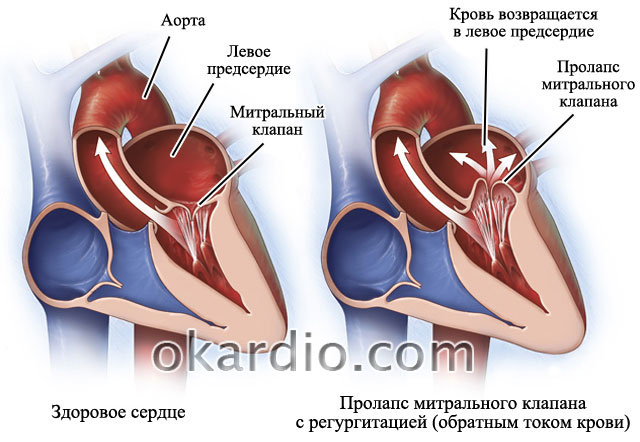 מחלת לב מיטראלית
מחלת לב מיטראלית גם שילובים של מחלות יכולים להיות הסיבה. לדוגמה, ניתן לשלב מומי לב עם מחלת לב כלילית (מחלת לב כלילית, אנגינה פקטוריס) ויתר לחץ דם עורקי (לחץ דם גבוה).
המצב לאחר ניתוח לב עלול לגרום לפרפור פרוזדורים, מכיוון שאחרי הניתוח עלולים להתרחש הדברים הבאים:
שינויים בהמודינמיקה תוך-לבבית (לדוגמה, היה מסתם רע - הושתל טוב, שהתחיל לפעול כהלכה).
חוסר איזון אלקטרוליטים (אשלגן, מגנזיום, נתרן, סידן). איזון אלקטרוליטיםמספק יציבות חשמלית לתאי הלב
דלקת (עקב תפרים בלב).
2. סיבות שאינן לבביות
צריכת אלכוהול עלולה להשפיע על הסיכון לפרפור פרוזדורים. במחקר שנערך על ידי מדענים אמריקאים ב-2004, הוכח כי עם עלייה במינון האלכוהול מעל 36 גרם ליום, הסיכון לפתח פרפור פרוזדורים עולה ב-34%. מעניין גם שמינוני אלכוהול מתחת לנתון זה אינם משפיעים על התפתחות AF.
דיסטוניה צמחונית היא קומפלקס של הפרעות תפקודיות של מערכת העצבים. עם מחלה זו, לעיתים קרובות מתרחשת הפרעת קצב התקפית (תיאור של סוגי הפרעות הקצב נמצא בבלוק הבא).
סיווג ותסמינים של AF
ישנם עקרונות רבים לסיווג FP. הנוח והמקובל ביותר הוא הסיווג המבוסס על משך פרפור פרוזדורים.
* פרוקסיזמים הם התקפים שעלולים להתרחש ולהיפסק באופן ספונטני (כלומר, באופן עצמאי). תדירות ההתקפות היא אינדיבידואלית.
תסמינים אופייניים
לכל סוגי הפרפור יש תסמינים דומים. כאשר פרפור פרוזדורים מתרחש על רקע המחלה הבסיסית, לרוב חולים מציגים את התלונות הבאות:
- דפיקות לב (קצב תכוף, אבל עם צורה ברדיסיסטולית, קצב הלב, להיפך, נמוך - פחות מ-60 פעימות לדקה).
- הפרעות ("דהייה" של הלב ולאחר מכן עוקב אחר הקצב, אשר עשוי להיות תכוף או נדיר). קצב תכוף - יותר מ-80 פעימות לדקה, נדיר - פחות מ-65 פעימות לדקה).
- קוצר נשימה (נשימה מהירה וקשה).
- סְחַרחוֹרֶת.
- חוּלשָׁה.
אם פרפור פרוזדורים קיים במשך זמן רב, אז מתפתחת בצקת ברגליים, עד הערב.
אבחון
אבחון פרפור פרוזדורים אינו קשה. האבחנה נקבעת על בסיס א.ק.ג. כדי להבהיר את תדירות ההתקפים ושילוב עם הפרעות קצב אחרות, מתבצעת אחת מיוחדת (ניטור א.ק.ג. במהלך היום).
 פעימות לב באלקטרוקרדיוגרמה. לחץ על התמונה להגדלה
פעימות לב באלקטרוקרדיוגרמה. לחץ על התמונה להגדלה  א.ק.ג משמש לאבחון פרפור פרוזדורים
א.ק.ג משמש לאבחון פרפור פרוזדורים טיפול בפרפור פרוזדורים
הטיפול מכוון לסילוק הגורם ו/או מניעת סיבוכים. במקרים מסוימים אפשר להחזיר את קצב הסינוס, כלומר לרפא פרפור, אבל קורה גם שלא ניתן להחזיר את הקצב - במקרה זה חשוב לנרמל ולתחזק את עבודת הלב, כדי למנוע את התפתחות של סיבוכים.
כדי לטפל בהצלחה ב-AF, אתה צריך: לחסל את הסיבה שגרמה להפרעות קצב, לדעת את גודל הלב ואת משך ההבהוב.
בבחירת שיטת טיפול כזו או אחרת, המטרה נקבעת תחילה (בהתאם למצבו הספציפי של המטופל). זה חשוב מאוד, שכן טקטיקה ומערכת של אמצעים יהיו תלויים בזה.
בתחילה, הרופאים רושמים תרופות, במקרה של חוסר יעילות - טיפול בדחפים חשמליים.
כאשר טיפול תרופתי, אלקטרופולס, אינו עוזר, הרופאים ממליצים (טיפול מיוחד בגלי רדיו).
טיפול רפואי
אם ניתן להחזיר את הקצב, אז הרופאים יעשו כל מאמץ לעשות זאת.
תרופות המשמשות לטיפול ב-AF מוצגות בטבלה. המלצות אלו מקובלות בדרך כלל להקלה על פרפור פרוזדורים.
טיפול באלקטרופולס
לפעמים הטיפול בתרופות (תוך ורידי או טבליות) הופך ללא יעיל, ולא ניתן להחזיר את הקצב. במצב כזה מתבצע טיפול באלקטרופולס - זוהי שיטה להשפעה על שריר הלב בפריקה של זרם חשמלי.
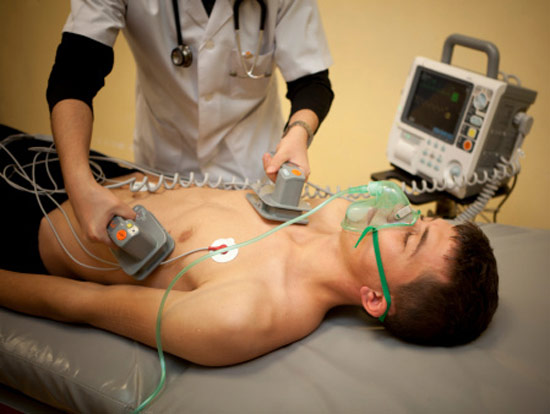 טיפול באלקטרופולס
טיפול באלקטרופולס ישנן שיטות חיצוניות ופנימיות:
החיצוני מתבצע דרך העור והחזה. שיטה זו נקראת לעיתים ה-Cardioversion. פרפור פרוזדורים מפסיק ב-90% מהמקרים אם הטיפול מתחיל בזמן. בבתי חולים לניתוחי לב, הגברת הלב יעילה מאוד ומשמשת לעתים קרובות להפרעות קצב התקפיות.
פְּנִימִי. צינור דק (קטטר) מוחדר לחלל הלב דרך הוורידים הגדולים של הצוואר או באזור עצם הבריח. אלקטרודה מועברת דרך הצינור הזה (בדומה לחיווט). ההליך מתרחש בחדר הניתוח, שם, תחת שליטה של רדיוגרפיה, הרופא יכול להעריך חזותית על המסכים כיצד לכוון ולהתקין כראוי את האלקטרודה.
לאחר מכן, בעזרת ציוד מיוחד המוצג באיור, מוחל פריקה והם מסתכלים על המסך. על המסך, הרופא יכול לקבוע את אופי הקצב (קצב הסינוס התאושש או לא). פרפור פרוזדורים מתמשך הוא המקרה הנפוץ ביותר כאשר רופאים משתמשים בטכניקה זו.
אבלציה RF
כאשר כל השיטות אינן יעילות, ופרפור פרוזדורים מחמיר משמעותית את חיי המטופל, מומלץ לבטל את הפוקוס (שקובע את הקצב השגוי ללב) שאחראי לעלייה בתדירות ההתכווצויות - אבלציה בתדר רדיו (RFA) - טיפול בגלי רדיו.
 אבלציה RF
אבלציה RF לאחר ביטול הפוקוס, הקצב עשוי להיות נדיר. לכן ניתן לשלב RFA עם השתלת קוצב לב מלאכותי - קוצב לב (אלקטרודה קטנה לתוך חלל הלב). קצב הלב דרך האלקטרודה יקבע על ידי קוצב לב, המותקן מתחת לעור באזור עצם הבריח.
עד כמה השיטה הזו יעילה? אם RFA בוצע על מטופל עם AF התקפי, אזי קצב הסינוס נשמר ב-64-86% מהחולים במהלך השנה (נתוני 2012). אם הייתה צורה מתמשכת, אז פרפור פרוזדורים חוזר במחצית מהמקרים.
מדוע לא תמיד ניתן להחזיר את קצב הסינוסים?
הסיבה העיקרית לאי היכולת לשחזר את קצב הסינוס היא גודל הלב והאטריום השמאלי.
אם, על פי האולטרסאונד של הלב, גודל הפרוזדור השמאלי הוא עד 5.2 ס"מ, אז ב-95% אפשרי שחזור קצב הסינוס. כך מדווחים רופאי קצב וקרדיולוגים בפרסומים שלהם.
כאשר גודל הפרוזדור השמאלי גדול מ-6 ס"מ, שחזור קצב הסינוס אינו אפשרי.
 אולטרסאונד של הלב מראה שגודל הפרוזדור השמאלי הוא יותר מ-6 ס"מ
אולטרסאונד של הלב מראה שגודל הפרוזדור השמאלי הוא יותר מ-6 ס"מ למה זה קורה? כאשר חלק זה של הלב נמתח, מתרחשים בו כמה שינויים בלתי הפיכים: פיברוזיס, ניוון של סיבי שריר הלב. שריר לב כזה (השכבה השרירית של הלב) לא רק שאינו מסוגל לשמור על קצב סינוס למשך שניות, אלא, לדברי קרדיולוגים, אסור לעשות זאת.
תַחֲזִית
אם AF מאובחנת בזמן, והמטופל ממלא אחר כל המלצות הרופא, אזי הסיכויים לשחזר את קצב הסינוס גבוהים - יותר מ-95%. אנו מדברים על מצבים שבהם גודל הפרוזדור השמאלי אינו עולה על 5.2 ס"מ, ולמטופל יש הפרעת קצב או הפרוקסיזם של פרפור פרוזדורים שאובחנו לאחרונה.
קצב הסינוס, שניתן לשחזר לאחר RFA בחולים עם צורה מתמשכת, נמשך שנה ב-50% מהמקרים (מכלל החולים שעברו ניתוח).
אם הפרעת הקצב קיימת מספר שנים, למשל, יותר מ-5 שנים, וללב יש גודל "גדול", אז המלצות הרופאים הן טיפול תרופתי שיעזור לעבודתו של לב כזה. לא ניתן לשחזר את הקצב.
ניתן לשפר את איכות החיים של חולים עם AF אם יש לעקוב אחר הטיפול המומלץ.
אם הסיבה היא אלכוהול ועישון, אז זה מספיק כדי לחסל את הגורמים האלה כדי שהקצב יחזור לקדמותו.
בבסיסה, ניתן לייחס מחלה זו להפרעת קצב לב, ה"מנוע האנושי" במקום התכווצויות רגילות מייצר כאוטיים ולא קצביים. פרפור מסווג לשתי צורות:
אם לשפוט לפי השם, קל להבין שמוקד הלוקליזציה של צורת החדר הוא בחדרי הלב, והמוקד של הצורה השנייה הוא הפרוזדור. אם נצפים התכווצויות תכופות של דחפים באטריום, אז הם תמיד פוגעים בחדרים.
כלומר, אם מבחינים בהפרות בצורה הראשונה, אז הן משפיעות על האחר. עם זאת, הרופאים מפרידים בין צורות אלו על מנת לציין במדויק את מוקד המחלה.
כיצד מסווגים פרפורים?
בְּ אדם בריאתדירות ההתכווצויות של שריר הלב נע בין 60 ל-80 פעמים בדקה. אם הפרוזדורים מתכווצים תוך דקה מ-200 עד 650 פעמים, וחדרי הלב מ-200 עד 500 פעמים, אז מתרחשת הפרוקסיזם של פרפור פרוזדורים.
מחלה כזו יכולה להיות משני סוגים:
בסוג הראשון קיימת תדירות התכווצויות גבוהה מאוד, עד כ-600 לדקה, בעוד שריר הלב מתכווץ בזמן עם החדר, כלומר עבודת הלב היא לא יציבה לחלוטין. עם רפרוף, התכווצות פרוזדורים מגיעה ל-400 פעמים בדקה, חדרי הלב מתכווצים עם הפרוזדור, אך במידה פחותה, הקצב הכללי ממשיך לתפקד בצורה מאוזנת.
אם ניקח בחשבון את הקשר בין IHD לפרוקסיזם של פרפור פרוזדורים, אז נוכל לציין את הדברים הבאים - מחלת לב איסכמית, כמו גם פרפור, היא תהליך פתולוגי שמוביל להפרעה במערכת האחראית על זרימת הדם. על רקע מחלות אלו מתפתחות הפרעות שונות, ביניהן הפרעות קצב לב.
זנים של המחלה
ברפואה, הפרעת קצב מחולקת למספר סוגים, תוך התחשבות במאפייני המחלה:
- התקפי. טופס זה מאובחן עבור אותם חולים בהם התקף הפרפור אינו חולף במהלך היום. או אם טיפול דחוף, בצורה של הילוכים מלאכותיים, לא עזר להחזיר את קצב הלב.
- מַתְמִיד. קטגוריה זו מוקצית לאותם חולים שההתקף שלהם לא חולף במשך 10 ימים, והשימוש בטיפול תרופתי עוזר לשחזר את התכווצות פרוזדורים למשך מספר ימים בלבד.
- קָבוּעַ. הצורה האחרונה היא הקשה ביותר, הילוכים לא עוזרים להחזיר את קצב ההתכווצות, החולים מרגישים כל הזמן התקפי פרפור.
מהי הסכנה של מחלה
הלב האנושי חייב לשחק את התפקיד של מה שנקרא משאבה, אשר מזרימה דם ללא הרף, יתר על כן, בצורה חלקה ושווה מעל מערכת כלי הדם. בתהליך זה חודרים חומרים מזינים וחמצן לכל הרקמות והאיברים, ופחמן דו חמצני וחומרים רעילים מוסרים מהגוף. גוף האדם. "משאבת" הלב מורכבת מארבע מחלקות עיקריות:
- אטריום שמאל;
- חדר ימני;
- שני חדרי לב.
כל המחלקות מעורבות בעבודה, שחייבות לבצע צירים בצורה מתואמת, כלומר התדירות - הן של החדרים והן של הפרוזדורים - חייבת להיות זהה בהכרח. אם הצירים יהיו כאוטיים, איברים אנושיים לא יוכלו לקבל חמצן וחומרי מזון בכמות מספקת, ובעיקר יסבלו מערכת עצביםוהמוח. ואם אספקת הדם תפסיק ל-5 דקות, זה יוביל למוות.
אילו סימנים קליניים עשויים להצביע על התפתחות פתולוגיה
התסמינים הקליניים של פרפור דומים לסימנים של הפרעת קצב לב. לרוב, מטופלים מרגישים:
- עלייה בקצב הלב;
- כאב ותחושת כובד בחזה;
- חולשה בכל הגוף וסחרחורות תכופות;
- אצל מטופל, העור הופך חיוור, קצב הנשימה עולה;
- בכל רגע הם מסוגלים לאבד את ההכרה, לפעמים נצפה פעימה על כלי צוואר הרחם.
עם הביטוי של הסימנים לעיל, עליך לקבוע תור לרופא בהקדם האפשרי על מנת לעבור בדיקה מקיפה, שעל בסיס תוצאותיה ייקבע טיפול יעיל.
מה הבסיס לטיפול במחלה
קודם כל, הרופא ירשום מחקרים קליניים כדי לזהות את צורת הפרפור. אם יאושר כי יש צורך לטפל בפרפור פרוזדורים התקפי, החולה יצטרך להפסיק, במיוחד אם התקף זה הוא הראשון בחייו של המטופל.
לטיפול, נרשמה תרופה שיכולה לעצור התקף ללא בעיות. התרופה נגד הפרעות קצב שנקבעה לרוב תרופותכגון אמיודרון או פרופאנון. זה האחרון נקבע ברוב המקרים, מכיוון שלתרופה יש הרכב עדין יותר, ובמקביל יש לה יעילות טיפולית גבוהה. התרופה מתחילה את פעולתה תוך שעה לאחר בליעה, השפעה מקסימליתמגיע תוך 2.5-3 שעות, סגולות רפואיות נמשכות למשך 9-12 שעות.
אם לחולה יש צורה קבועה של המחלה, אז הוא רושם טיפול תרופתי עם תרופות שייבחרו בנפרד. אתה צריך לקחת תרופות כל הזמן כדי לשלוט בקצב הלב שלך ולמנוע שבץ. כלומר, טיפול תרופתי ייכנס הן כמניעה מפני סיבוכים, והן כטכניקת טיפול יעילה עוצמתית.
התרופות היעילות ביותר שבאמצעותן הפסקת הפרעות קצב הן הבאות:
איזו תרופה יש לרשום למטופל צריך להחליט רק על ידי הרופא המטפל, תוך התחשבות בשלב התפתחות המחלה ואי סבילות אינדיבידואלית לתרופות. בנוסף, אין לשכוח שחלק מהתרופות חייבות להינתן תוך ורידי, בעוד שאחרות יש לשתות לפני או אחרי הארוחות. איזו שיטה תהיה היעילה ביותר, רק הרופא צריך להחליט.
טיפול חירום ב-AF תלוי בעיקר בביטוי של ביטויים קליניים. הרפואה המודרנית לא עומדת במקום, שואפת להתפתח כל הזמן, מציגה את השיטות העדכניות ביותר לטיפול במחלות לב. זה כבר צוין יעיל מאוד ו שיטה בטוחהלחסל הפרעת קצב, המבוססת על אבלציה של צנתר בתדר רדיו. נכון לעכשיו, טכניקת טיפול זו משמשת הן לנרמל את קצב הסינוס והן להפחתת פרפור פרוזדורים. מטופלים לאחר RFA מרגישים טוב, קצב הלב שלהם משוחזר, הם מתאוששים במהירות.
אילו סיבוכים יכולים לגרום לפרפור פרוזדורים?
אם לא מטפלים בפרפור, הסיכון לאוטם שריר הלב או שבץ מוחי גדל מאוד. העובדה היא שעם צורה זו של הפרעת קצב, שריר הלב אינו יכול להתכווץ כרגיל, כתוצאה מכך, הדם עומד באטריום, מה שמעורר היווצרות של קרישי דם.
עם הזמן, פקקת מסוגלת להיכנס לעורק, לסתום אותו או איבר אחר אליו הוא יועבר על ידי זרימת הדם, ואם הוא נפגע. עורקים המספקים דם ללב, אז עלולה להתפתח מחלת עורקים כליליים. בנוסף למחלות אלה, פרפור מוביל לתוצאות הבאות:
רק ביקור בזמן אצל הרופא ושיטה שנבחרה נכון לטיפול בפרפור פרוזדורים יקל על מצבו של המטופל וימנע את התרחשותם של סיבוכים מסוכנים.
פרפור פרוזדורים: גורמים, צורות, ביטויים, אבחון, משטרי טיפול, פרוגנוזה
פרפור פרוזדורים הוא סוג של הפרעת קצב שבה הפרוזדורים מתכווצים בקצב של דקה, אך רק חלק מהדחפים מגיעים לחדרים, מה שיוצר את התנאים המוקדמים לפעילותם הבלתי מסודרת ומתבטא באי סדירות של הדופק.
פרפור פרוזדורים נחשב לאחת הגרסאות הנפוצות ביותר של הפרעות קצב לב. היא מופיעה בכל מקום, בעיקר בקרב אנשים בגיל בוגר וקשישים, ועם השנים, הסבירות להפרעות קצב רק עולה. לפתולוגיה יש לא רק חשיבות סוציו-רפואית רבה בשל הסיכון הגבוה לסיבוכים קשים ומוות, אלא גם כלכלית, שכן היא דורשת עלויות חומריות משמעותיות למניעה וטיפול.
לפי הסטטיסטיקה, פרפור פרוזדורים מהווה עד 2% מכלל הפרעות קצב הלב, ומספר החולים גדל ללא הרף עקב ההזדקנות הכללית של אוכלוסיית העולם. עד גיל 80 השכיחות של פרפור פרוזדורים מגיעה ל-8%, ובגברים הפתולוגיה מתבטאת מוקדם יותר ולעתים קרובות יותר מאשר אצל נשים.
פרפור פרוזדורים מסבך לעתים קרובות מאוד אי ספיקת לב כרונית, אשר בתורה משפיעה על רוב האנשים עם מחלת עורקים כליליים. לפחות רבע מהחולים אי ספיקה כרוניתיש כבר אבחנה של פרפור פרוזדורים. ההשפעה המשולבת של מחלות אלו גורמת להחמרה הדדית של המהלך, להתקדמות ולפרוגנוזה רצינית.
שם נפוץ נוסף לפרפור פרוזדורים הוא פרפור פרוזדורים, הוא נפוץ יותר בקרב חולים, אך גם אנשי מקצוע רפואיים משתמשים בו באופן פעיל. הניסיון המצטבר בטיפול בפתולוגיה זו מאפשר לא רק לחסל הפרעות קצב, אלא גם למנוע בזמן הפרוקסיזם של פרפור פרוזדורים וסיבוכים שלהם.
היווצרות מסודרת של דחפים בצומת הסינוס, מעוררת התכווצות לב בנורמה (משמאל) ופעילות חשמלית כאוטית בפרפור פרוזדורים (ימין)
שימו לב שהמונח "פרפור פרוזדורים" יכול להתייחס לשני סוגים של הפרעות קצב פרוזדוריות:
- במקרה אחד הם מתכוונים לפרפור פרוזדורים (פרפור פרוזדורים), המתואר להלן, כאשר דחפים בתדירות גבוהה מתפשטים באקראי בשריר הלב שלהם, וכתוצאה מכך רק סיבים בודדים מתכווצים במהירות ובאופן לא עקבי במיוחד. יחד עם זאת, החדרים מתכווצים בהפרעות קצב וביעילות לא מספקת, מה שמוביל להפרעות המודינמיות.
- במקרה אחר הכוונה לרפרוף פרוזדורים, כאשר סיבי שריר הלב מתכווצים לאט יותר - בתדירות של דקה. בניגוד להבהוב (פרפור), עם רפרוף פרוזדורים, הם עדיין מתכווצים, ורק חלק מהדחפים מגיעים לשריר הלב החדרים, ולכן הם "עובדים" לאט יותר. בשני המקרים, יעילות הלב פוחתת, ואי ספיקת מחזור הדם מתקדמת.
וידאו: בסיסי על פרפור פרוזדורים + דבש. אנימציה
צורות של פרפור פרוזדורים
בהתאם לסיווג המודרני, קיימות מספר צורות של פרפור פרוזדורים:
- בפעם הראשונה התעורר - הפרק הראשון שהוקלט של הפרעת קצב, כאשר לא ניתן לקבוע את הסבירות להישנות.
- צורה פרוקסימלית של פרפור פרוזדורים - מתרחשת בצורה של פרקים תכופים יותר או פחות של הפרעה בקצב, המשוחזרת תוך לא יותר משבוע.
- פרפור מתמשך (חוזר) - נמשך יותר מ-7 ימים ודורש היפוך כושר.
- צורה קבועה - אי אפשר או לא נדרש להחזיר את הקצב.
למתרגל חשוב לקבוע את הצורה הראשונה של פרפור, עם זאת, לא תמיד ניתן לקבוע את משך הזמן שלה ולא לכלול את העובדה של אפיזודות קודמות של הפרעת קצב.
כאשר מתבססת הפרוקסיזם שני או יותר של הפרעות בקצב פרוזדורים, מאובחנת צורה מתמשכת של פרפור פרוזדורים. אם הקצב מסוגל להתאושש באופן ספונטני, אז הפרעת קצב מתמשכת (חוזרת) כזו תיקרא הפרוקסיזמלית, והמונח "מתמשך" ישמש כאשר היא נמשכת יותר משבעה ימים. הפרעת קצב שזוהתה לראשונה יכולה להיות גם התקפית וגם מתמשכת.
צורה קבועה של פרפור פרוזדורים (קבוע) אמורה להיות כאשר הפרעת הקצב נמשכת יותר משנה, אך לא הרופא ולא המטופל מתכננים להחזיר את הקצב באמצעות קרדיו-הורסיה. במקרה בו האסטרטגיה הטיפולית משתנה, הפרעת הקצב נקראת מתמשכת ארוכת טווח.
בהתאם לקצב הדופק, קיימות שלוש צורות של פרפור פרוזדורים:
- טכיסיסטולי - יותר דחפים מקוצבי לב פרוזדורים מגיעים לחדרים מהנדרש בדרך כלל, וכתוצאה מכך הדופק מגיע לפעימות בדקה או יותר.
- פרפור ברדיסיסטולי - תדירות ההתכווצויות של החדרים אינה מגיעה ל-60.
- נומוסיסטולי - החדרים מתכווצים בתדירות קרובה לנורמה, - פעימות לדקה.
הסיבות
פרפור פרוזדורים יכול להתרחש הן ללא סיבה ברורה והן עם מספר מצבים התורמים לפתולוגיה:
קרדיווסקלרוזיס ונגעים אורגניים אחרים בשריר הלב הם הגורמים השכיחים ביותר לפרפור פרוזדורים
סוג מבודד של פרפור (מחוץ למחלת לב) מאובחן בדרך כלל בצעירים, ופתולוגיה לבבית נלווית מאפיינת הפרעות קצב לעיתים קרובות יותר אצל קשישים.
גורמי סיכון שאינם לבביים לפרפור פרוזדורים הם תפקוד מוגבר של בלוטת התריס, עודף משקל, סוכרת, פתולוגיה כלייתית, תהליכים חסימתיים כרוניים בריאות, נגעים התחשמלות, עבר ניתוח לב, שימוש לרעה באלכוהול. בנוסף, אפשרית השפעה של גורם תורשתי ומוטציות גנטיות (זוג X של כרומוזומים): כשליש מהחולים עם פרפור יש הורים עם אותה צורה של הפרעת קצב לב.
גילויים
תסמינים של פרפור פרוזדורים נקבעים לפי הצורה ומהלך הפתולוגיה. אפשריים גם מהלך אסימפטומטי וגם כשל חמור במחזור הדם עם תסמינים עזים. חלק מהחולים, לא רק עם הצורה הפרוקסיזמלית, אלא גם עם הצורה הקבועה, אינם מתלוננים כלל, באחרים הפרק הראשון של הפרעת קצב יכול להתבטא בהפרעות המודינמיות חמורות עד בצקת ריאות, תסחיף מוחי וכו'.
התלונות השכיחות ביותר בפרפור פרוזדורים הן:
- אי נוחות בחזה או אפילו כאב באזור הלב;
- קרדיופלמוס;
- חוּלשָׁה;
- סחרחורת והתעלפות עם תת לחץ דם חמור;
- קוצר נשימה עם אי ספיקה גוברת של החדר השמאלי של הלב;
- הטלת שתן תכופה.
במהלך תקופת הפרוקסיזם של הפרעת קצב או עם צורה קבועה, המטופל עצמו חוקר את הדופק ומרגיש את אי הסדירות שלו. במקרה של טכיסיסטולה חמורה, מספר ההתכווצויות יעלה על קצב הפעימה בעורקים ההיקפיים, הנקרא חוסר דופק.
מהלך הפתולוגיה מושפע מנפח הפרוזדור השמאלי: עם עלייתו כתוצאה מהרחבת החלל, קשה לשמור על הקצב לאחר הקרדיוורסיה. מחלות שבהן שריר הלב הפרוזדור השמאלי נפגע מלוות יותר בפרפור מאשר שינויים בחלקים אחרים של הלב.
אצל מטופלים רבים הסובלים מכל אחת מהגרסאות של פרפור פרוזדורים, איכות החיים משתנה. עם צורה קבועה או עם ההתקף הבא של הפרעת קצב, זה מוגבל פעילות גופנית, בהדרגה, עקב התקדמות אי ספיקת לב, סובלנות הפעילות הגופנית פוחתת, ולכן ייתכן שיהיה צורך לשנות את הסוג פעילות עבודה, דחייה פעילויות ספורט, נסיעות ארוכות וטיסות.
אפילו עם מהלך אסימפטומטי או בולט מינימלי של המחלה, הסימן הראשון לפתולוגיה יכול להיות שבץ קרדיו-אמבולי (כאשר קריש דם נוצר באטריום עקב "הבהוב" מתמיד של קריש דם נכנס לעורקים המזינים את המוח) . במקרים אלו יבואו לידי ביטוי ביטויים נוירולוגיים (פארזיס, שיתוק, תרדמת, הפרעות תחושתיות ועוד) ובפעם השנייה תאובחן הפרעת קצב, אם תופיע בפעם הראשונה.
כשלעצמו, פרפור פרוזדורים יכול להימשך זמן רב באופן שרירותי מבלי לגרום לאי נוחות משמעותית לסובל, עם זאת, סיבוכים של הפתולוגיה יכולים להחמיר מאוד את המצב. בין הנפוצים ביותר ובו בזמן, השלכות מסוכנותהפרעה בקצב פרוזדורי (יחד עם תסמונת תרומבואמבולית עם סיכון לאוטם מוחי) - הגברת אי ספיקת לב חמורה עם פירוק מהיר למדי, בצקת ריאות על רקע הפרעה חריפה של החדר השמאלי.
אבחון וסימני אק"ג של פרפור פרוזדורים
אם יש חשד לפרפור חדרים, גם אם ההתקף אירע רק לטענת המטופל, והפסיק עד למועד הבדיקה, יש צורך בבדיקה יסודית. לשם כך, הרופא שואל בפירוט על אופי התלונות והתסמינים, זמן הופעתם והקשר ללחץ, מגלה אם המטופל סובל מכל פתולוגיה לבבית אחרת או אחרת.
בדיקות לגילוי חשד לפרפור חדרים יכולות להתבצע באישפוז, אם כי במקרה של התקף ראשוני, האמבולנס יעדיף לקחת את המטופל לבית החולים לאחר ביצוע קרדיוגרמה המאשרת את הימצאות הפרעת קצב.
בְּ בדיקה ראשוניתהרופא מתקן את אי הסדירות של הדופק, חירשות של גווני הלב, טכיקרדיה עם טכיפורם. לאחר מכן מבוצעים מחקרים אינסטרומנטליים נוספים כדי לאשר את הפרעת הקצב - א.ק.ג, אקו לב, ניטור יומי.
לפרפור פרוזדורים ב-ECG יש מספר מאפיינים אופייניים:
- היעלמותו של גל P עקב היעדר התכווצויות פרוזדוריות מתואמות;
- גלים f, המאפיינים התכווצויות של סיבים בודדים ובעלי גודל וצורה משתנים;
- מרווחי RR בעלי משך שונה עם קומפלקס חדרים ללא שינוי.
כדי לאשר פרפור פרוזדורים, צריכים להיות שינויים אופייניים בלפחות א.ק.ג אחד. אם בזמן המחקר ההתקף נפסק, אזי יוצע למטופל לעבור ניטור יומי.
אקו-לב יכול לזהות פגמים במסתמים, פקקים תוך-אטריאליים, מוקדים של שינויים מבניים בשריר הלב. בנוסף למחקרי לב, מוצגות בדיקות להורמוני בלוטת התריס, תפקודי כבד וכליות והרכב האלקטרוליטים של הדם.
סרטון: שיעור א.ק.ג. להפרעות קצב לא-סינוסיות, פרפורים ורפרופים
עקרונות הטיפול בפרפור פרוזדורים
בתכנון הטיפול בפרפור פרוזדורים עומדת בפני הרופא בחירה: לנסות להשיג את החזרת הקצב הנכון, או לשמור על הפרעת הקצב, אך עם קצב לב תקין. מחקרים עדכניים מראים ששתי אפשרויות הטיפול טובות, ושליטה בדופק, גם בנוכחות הפרעת קצב, משפרת את שיעורי ההישרדות ומפחיתה את שכיחות התרומבואמבוליזם כסיבוכים.
הטיפול בחולים עם פרפור פרוזדורים נועד להעלים את התסמינים השליליים של הפרעות קצב ולמנוע סיבוכים חמורים. עד כה, אומצו והשתמשו בשתי אסטרטגיות לניהול חולים:
- בקרת קצב הלב - שחזור קצב הסינוס ומניעת חזרת הפרעת קצב תרופתית;
- שליטה בקצב הלב (קצב הלב) - הפרעת קצב נמשכת, אך קצב הלב מואט.
כל האנשים עם אבחנה מבוססת של הפרעת קצב, ללא קשר לאסטרטגיה שנבחרה, מקבלים טיפול נוגד קרישה למניעת היווצרות פקקת פרוזדורים, שהסיכון לכך גבוה מאוד בפרפור פרוזדורים, הן קבועות והן במהלך הפרוקסיזם. בהתבסס על ביטויים של הפרעת קצב, גיל, פתולוגיה נלוויתתכנית טיפול נעשתה על בסיס אישי. זה יכול להיות קרדיוורסיה, תחזוקה של תרופות לדופק היעד, מניעה של אפיזודות חוזרות של פרפור ותסמונת תרומבואמבולית היא חובה.
טיפול נוגד קרישה
פרפור פרוזדורים מלווה בסיכון גבוה ביותר לפקקת עם תסחיף במעגל גדול וביטוי של הסיבוכים המסוכנים ביותר, בפרט, שבץ תסחפי, ולכן חשוב מאוד לרשום טיפול נוגד קרישה - נוגדי טסיות, נוגדי קרישה ישירים או עקיפים. פעולה.
אינדיקציות למינוי נוגדי קרישה הן:
- גיל עד 60 שנים, כאשר אין נזק מבני בשריר הלב או איתו, אך ללא גורמי סיכון, יש לציין חומצה אצטילסליצילית;
- לאחר 60 שנה, אך ללא גורמים נוטים - אספירין, קרדיומגניל נקבעים;
- לאחר 60 שנה, עם סוכרת מאובחנת או מחלת לב כלילית, התווית וורפרין בשליטה של INR, שילוב עם אספירין אפשרי;
- בגיל 75 ומעלה, במיוחד נשים, כמו גם עם מחלות נלוות קשות (תירוטוקסיקוזיס, אי ספיקת לב, יתר לחץ דם), וורפרין נקבע;
- מחלת לב ראומטית, ניתוחי מסתמים, פקקת או תסחיף קודמים מחייבים שימוש חובה בוורפרין.
טיפול נוגד קרישה כולל:
- נוגדי קרישה עקיפים - warfarin, pradaxa - נקבעים במשך זמן רב בשליטה של קרישה (INR בדרך כלל 2-3);
- תרופות נוגדות טסיות - חומצה אצטילסליצילית(טרומבו תחת, אספרין קרדיו וכו') במינון של 325 מ"ג, דיפירידמול;
- הפרינים במשקל מולקולרי נמוך - משמשים במצבים אקוטיים, לפני היפוך קיבה, מפחיתים את משך השהייה בבית החולים.
יש לזכור ששימוש ארוך טווח במדללי דם עלול לגרום תופעות לוואיבצורת דימום, לכן, אנשים עם סיכון מוגבר לסיבוכים כאלה או ירידה בקרישה בהתאם לתוצאות של קרישה, נוגדי קרישה נקבעים בזהירות רבה.
א. אסטרטגיית בקרת קצב
אסטרטגיית בקרת הקצב כוללת את השימוש סוכנים תרופתייםאו הסבה חשמלית כדי להחזיר את הקצב הנכון. בצורת הטכיסיסטולית של הפרעת קצב, לפני החזרת הקצב הנכון (התכונה לבבית), יש צורך להפחית את קצב הלב, עבורם נקבעים חוסמי בטא אדרנרגיים (מטופרולול) או אנטגוניסטים של סידן (וראפמיל). בנוסף, קרדיוורסיה מצריכה טיפול חובה בנוגדי קרישה, מכיוון שההליך עצמו מגדיל באופן משמעותי את הסיכון לפקקת.
הסבה חשמלית
קרדיוורסיה חשמלית - נורמליזציה של הקצב באמצעות זרם חשמלי. שיטה זו יעילה יותר מהחדרת תרופות, אך גם כואבת יותר, ולכן חולים מקבלים תרופות הרגעה או מבצעים הרדמה כללית שטחית.
שחזור ישיר של קצב הסינוס מתרחש בפעולת קרדיווורטר-דפיברילטור, השולח דחף חשמלי ללב, המסונכרן עם גל R, כדי לא לגרום לפרפור חדרים. ההליך מיועד לחולים שבהם הכנסת חומרים תרופתיים אינה נותנת תוצאה או עם חוסר יציבות של זרימת הדם על רקע הפרעת קצב. בדרך כלל היא מתבצעת חיצונית, על ידי פעולת הפרשה על העור, אך יתכן גם היפוך תוך-לב אם שיטת השטח אינה יעילה.
ניתן לתכנן חילוף חומרים, ואז החולה לוקח וורפרין במשך 3 שבועות לפני ו-4 אחרי. הליך שחזור קצב מתוכנן נקבע למי שהפרעת הקצב שלו נמשכת יותר מיומיים או משך הזמן שלה אינו ידוע, אך ההמודינמיקה אינה מופרעת. אם הפרוקסיזם של הפרעת קצב נמשך פחות מ-48 שעות ומלווה בהפרעות חמורות בזרימת הדם (יתר לחץ דם, למשל), יש לציין העברת קרדיווסיה דחופה, בכפוף למתן חובה של הפרין או אנלוגים במשקל מולקולרי נמוך שלו.
קרדיווורסיה פרמקולוגית
Procainamide ניתן תוך ורידי, אך גורם לתופעות לוואי רבות - כאבי ראש, סחרחורת, יתר לחץ דם, הזיות, שינויים בנוסחת לויקוציטים, וזו הסיבה שהיא אינה נכללת ברשימת התרופות להפיכת הלב על ידי מומחים אירופאים. ברוסיה ובמדינות רבות אחרות, עדיין משתמשים בפרוקאינמיד בשל העלות הנמוכה של התרופה.
Propafenone זמין גם בתמיסה וגם בצורת טבליות. עם גרסה מתמשכת של פרפור פרוזדורים ורפרוף, אין לו את ההשפעה הרצויה, והוא גם אסור במחלות ריאות חסימתיות כרוניות ואינו רצוי מאוד לרישום לאנשים עם איסכמיה בשריר הלב והתכווצות חדר שמאל מופחת.
Amiodarone זמין באמפולות, ניתן לוריד ומומלץ לשימוש בנוכחות נגעים אורגניים בשריר הלב (צלקות לאחר אוטם, למשל), דבר שחשוב לרוב החולים הסובלים מפתולוגיה כרונית של הלב.
Nibentan זמין כפתרון לעירוי תוך ורידי, אך ניתן להשתמש בו רק במחלקות טיפול נמרץ, כאשר בקרת קצב אפשרית לאורך כל היום לאחר מתןה, שכן התרופה עלולה לעורר הפרעות קצב חדריות חמורות.
אינדיקציות ל-cardioversion תרופתית הן מקרים שבהם פרפור פרוזדורים התרחש בפעם הראשונה או מתרחשת התקפי הפרעת קצב עם קצב לב גבוה, המוביל לתסמינים שליליים ואי יציבות המודינמית, שלא מתוקן על ידי תרופות. אם הסבירות לשמירת קצב הסינוסים לאחר מכן קטנה, אז עדיף לסרב להתקף לב רפואי.
Cardioversion פרמקולוגי נותן התוצאות הטובות ביותר, אם הוא התחיל לא יאוחר מ-48 שעות לאחר הופעת התקף הפרעת קצב. התרופות העיקריות להפרעות קצב פרוזדוריות המתרחשות על רקע אי ספיקת לב גדושה נחשבות לאמיודרון ודופטיליד, שהן לא רק יעילות ביותר, אלא גם בטוחות, בעוד ששימוש ב-Novocainamide, Propafenone ותרופות אנטי-ריתמיות אחרות אינו רצוי עקב תופעות לוואי אפשריות. .
רוב כלי יעילאמיודרון נחשב כמחזיר את הקצב בפרפור פרוזדורים התקפי. על פי תוצאות מחקר, עם צריכת שנתיים של מטופלים עם אי ספיקת לב כרונית, התמותה הכוללת יורדת בכמעט מחצית, ההסתברות למוות פתאומי - ב-54%, והתקדמות של אי ספיקת לב - ב-40%.
ניתן לרשום תרופות נגד הפרעות קצב לאורך זמן על מנת למנוע הפרעות קצב חוזרות, אך במקרה זה יש לקחת בחשבון את הסיכון הגבוה לתופעות לוואי לצד יעילות נמוכה יחסית. שאלת הכדאיות של טיפול ארוך טווח מוכרעת באופן אינדיבידואלי, וסוטלול, אמיודרון, פרופאנון, אטציזין עדיפים לרישום.
ב. אסטרטגיית בקרת שיעורים
בבחירת אסטרטגיית שליטה על קצב הלב, לא פונים כלל להפיכת הלב, אך רושמים תרופות שמאטות את קצב הלב - חוסמי בטא (מטופרול, קרוודילול), חוסמי תעלות סידן (ורפמיל, דילטיאזם), אמיודרון עם חוסר יעילות של הקבוצות הקודמות.
התוצאה של האסטרטגיה הנבחרת צריכה להיות דופק לא גבוה מ-110 לדקה במנוחה. אם התסמינים בולטים, קצב הלב נשמר ברמה של עד 80 פעימות לדקה במנוחה ולא יותר מ-110 בפעילות גופנית מתונה. בקרת דופק מפחיתה את הביטויים של הפרעות קצב, מפחיתה את הסיכונים לסיבוכים, אך אינה מונעת את התקדמות הפתולוגיה.
ב. אבלציה בקטטר
אבלציה באמצעות תדר רדיו בצנתר (RFA) מסומנת כאשר המרת רדיו חשמלית ותרופתית אינה יעילה, או שהקצב התקין אינו נשמר על ידי תרופות אנטי-אריתמיות. RFA היא התערבות אנדווסקולרית זעיר פולשנית כאשר האלקטרודה מוחדרת דרך וריד הירך ולאחר מכן נשלחת אל הלב, שם הצומת האטריו-חדרי, סיבי צרור His נהרסים על ידי זרם חשמלי, או אזורי הדחפים הפתולוגיים בפתחים של ורידי הריאה מבודדים.
במקרה של הרס של הצומת האטrioventricular או צרור His, מתרחש חסימה רוחבית מלאה, כאשר הדחפים מהפרוזדורים אינם מגיעים לשריר הלב החדרי, לכן, אבלציה כזו מלווה בהתקנה של קוצב לב.
עם התפרצויות נדירות של פרפור פרוזדורים, אשר, לעומת זאת, מתרחשים עם תסמינים חמורים, ניתן להשתיל קרדיווורטר-דפיברילטורים תוך פרוזדורים, אשר אינם מונעים הפרעת קצב, אך למעשה מחסלים אותה אם היא מתרחשת.
מניעת הישנות של הפרעת קצב
מניעת התקפים חוזרים של פרפור פרוזדורים חשובה מאוד, שכן בלמעלה ממחצית מהמקרים הפרעת הקצב חוזרת בשנה הבאה לאחר קרדיוהורסיה, וניתן לשמור על קצב סינוס רק בשליש מהחולים.
יַעַד טיפול מונע- לא רק כדי למנוע אפיזודות חוזרות של הפרעות קצב, אלא גם כדי לעכב את התפתחות הגרסה הקבועה שלה, כאשר הסבירות לתסחיף, התקדמות של אי ספיקת לב ומוות פתאומי עולה באופן משמעותי.
למניעת התקף של פרפור פרוזדורים, מומלצים 3 חוסמי בטא - ביסופרולול, קרוודילול ומטופרולול. כדי לשמור על תקינות הקצב, עדיף לרשום אמיודרון.
תרופות להורדת שומנים בדם (סטטינים) בעלות השפעות מגנות לב, אנטי-איסכמיות, אנטי-פרוליפרטיביות ואנטי דלקתיות נכללות גם הן בתוכניות למניעת התקפים חוזרים של פרפור פרוזדורים. בחולים עם מחלת לב כלילית כרונית, סטטינים עוזרים להפחית את הסבירות להישנות הפרעת קצב.
הקלה על הפרוקסיזם של פרפור פרוזדורים מתבצעת תמיד במקרה של התרחשותו העיקרית. לשם כך, מבוצעת קרדיוורסיה באחת מהשיטות שתוארו לעיל, טיפול תרופתי בתרופות אנטי-ריתמיות נקבע במקביל לטיפול נוגד קרישה. חשוב במיוחד השימוש בנוגדי קרישה להפרעות קצב הנמשכות יותר מיומיים.
יש לספק טיפול חירום בהתקף של פרפור פרוזדורים עם עלייה בתסמינים של הפרעה בהמודינמיקה, בצקת ריאות, הלם קרדיוגני והשלכות חמורות אחרות של פעילות חשמלית לא תקינה של הלב. כאשר מצבו של המטופל אינו יציב (מחנק, כאבים חריפים בלב, תת לחץ דם חמור), יש לציין טיפול חירום באלקטרופולס, ועם מהלך יציב של הפרוקסיזם של הפרעת קצב, מתחיל תיקון קצב התרופה.
טיפול בפרפור פרוזדורים התקפי /PFFP/
רפובטס ולרי אלכסנדרוביץ'
קרדיולוג של מחלקת אוטם, מינסק
טיפול בהפרעות קצב לב הוא אחד הנושאים הבעייתיים של הקרדיולוגיה עקב היעדר גישה אחידה לטיפול בהפרעות קצב לב, כמו גם ביטוי של השפעה פרו-קצבית בתרופות האנטי-אריתמיות עצמן / AARP / - בממוצע עד 10 % מהמקרים. לא כל סוגי הפרעות הקצב דורשים טיפול חירום; במקביל, יש צורך לעבור בזמן משיטות טיפול שמרניות לניתוחיות. בגיל מעל 60 שנים, AF נצפה ב-5% מהאוכלוסייה, בקרב מעל גיל 75 - ב-14%. AF מדורגת במקום השני, אחרי extrasystoles, מבחינת השכיחות בקרב הפרעות קצב. בצפון אמריקה רשומים 2.2 מיליון חולים עם AF, באירופה - 4.5 מיליון. בגרמניה לבדה סובלים ממנה כמעט מיליון אנשים. עלות הטיפול בחולים עם AF במדינות האיחוד האירופי היא 13.5 מיליארד יורו בשנה (ACC/AHA/ESC).
ייתכן שהמטופל לא ירגיש AF או ירגיש זאת כפעימת לב. הדופק אינו סדיר . הצליל של הצלילים ניתן לשינוי. גם מילוי הדופק משתנה וחלק מהתכווצויות הלב, במיוחד לאחר הפסקות דיאסטוליות קצרות, אינו נותן גל דופק. בתנאים אלו, ניתן לקבוע את קצב הלב האמיתי רק באמצעות צלילי לב, בעוד שהתדירות הנקבעת על ידי מישוש הדופק נמוכה יותר (חסר דופק). פעילות גופנית מגבירה את תדירות התכווצויות החדרים ואת אי הסדירות שלהם. תסמינים אלה מרמזים על AF. פרפור פרוזדורים ארוך טווח עלול להוביל למתיחות פרוזדורים מסוימת שזוהתה בצילום רנטגן או אקו לב .
על גל א.ק.ג רחסר, הדיאסטולה מלאה בתצורה ובקצב לא סדיר של גלים קטנים, המורגשים יותר בעופרת V 1 . התדירות שלהם היא 300 - 600 לדקה (בדרך כלל זה לא סופר). קומפלקסים חדריים עוקבים בקצב הלא נכון, הם בדרך כלל אינם מעוותים. עם קצב חדרי שינה תכופים מאוד (יותר מ-150 פעימות לדקה), תיתכן חסימה של רגל ה-PG, בדרך כלל הימנית, של הצרור האטריו-חדרי. בהשפעת הטיפול, כמו גם בנוכחות הפרעות הולכה אטריונוטריקולרית יחד עם AF, התדירות של קצב החדר עשויה להיות נמוכה יותר. בתדירות של פחות מ-60 פעימות לדקה, הם מדברים על צורה ברדיסיסטולית של AF. מדי פעם, יש שילוב של AF עם חסימה אטריווצנטרית מלאה. יחד עם זאת, קצב החדר נדיר וקבוע. אצל אנשים עם PFFP, כאשר רושמים א.ק.ג מחוץ לפרוקסיזם, במיוחד זמן קצר לאחריו, מתגלה לעתים קרובות עיוות בולט יותר או פחות של השן. ר.
AF הוא סיבוך שכיח של מחלת לב מיטרלי, קרדיווסקלרוזיס טרשת עורקים, קרדיומיופתיה. גורמים חריפים (הפיכים) ל-AF: ניתוח (במיוחד בלב או בחזה), הלם חשמלי, אוטם שריר הלב חריף, דלקת שריר הלב, מחלת ריאות חריפה, PE. AF נצפה גם עם נזק חודרני לשריר הלב במסגרת עמילואידוזיס, המוכרומטוזיס, כמו גם עם גידולים של הלב. ב-AF שאובחן לאחרונה, יש לשלול תירוטוקסיקוזיס או תפקוד לקוי אחר של בלוטת התריס. נדונים גם גורמים נוספים - צניחת מסתם מיטרלי עם רגורגיטציה מיטראלית, הסתיידות של הטבעת המיטרלית והגדלה אידיופטית של פרוזדור ימין. בחולים מסוימים, במיוחד חולים צעירים יותר, AF עשויה להיות קשורה לנוכחות של טכיקרדיה על-חדרית התקפית נוספת, במיוחד לעיתים קרובות בנוכחות תסמונת קדם-אקסיטציה חדרית (PVS). טיפול מוצלח במחלה הבסיסית יכול לחסל AF. גורם סיכון נוסף הממריץ התפתחות של הפרעות קצב הוא צריכת אלכוהול. ידועה מה שמכונה "חופשת הלב" (Holiday-Heart-Syndroms) המאופיינת בהופעת הפרעות בקצב הלב אצל אנשים שותים ללא קרדיומיופתיה מאומתת לאחר צריכת אלכוהול מסיבית, למשל, בהזדמנויות שונות בסוף השבוע.
במקרים נדירים, AF נוירוגני נגרמת על ידי השפעות נרתיקיות או סימפטיות. זיהוי מנגנון כזה להופעת AF מאפשר לרופא לבחור חומר תרופתי שסביר יותר למנוע את הישנות הפרעת הקצב. נודע כי מוטציות בכרומוזום 10 (g22-24), כמו גם פולימורפיזם גנטי של אדרנורצפטורים אלפא ובטא, מובילים למקרים משפחתיים של פרפור פרוזדורים. זה הוכח לראשונה על ידי P. Brugada וחב' (1997), שתיאר שלוש משפחות. 21 מתוך 49 קרובי משפחה סבלו מ-AF, שניים מהם מתו בגיל 2 ו-46 מתאונה חריפה של כלי דם מוחיים. לפיכך, בהתבסס על תוצאות המחקרים הנ"ל, ניתן לטעון כי ל-AF עשויה להיות נטייה גנטית.
ב-30% מהמקרים, AF מתרחשת ללא מחלת לב קודמת.
1. התרחשות בפרוזדורים של מספר מוקדים של אוטומטיזם חוץ רחמי.
2. הפרה של הפונקציה של צומת הסינוס.
3.קיומם של מסלולים נוספים /תסמונת SVC/.
4. היפרטרופיה ועומס יתר של ה-LP.
5. שינוי במצב התפקודי של ה-NS המרכזי והוגטטיבי.
טבלה 1. גורמים אנטומיים ואלקטרופיזיולוגיים התורמים להופעת ו/או תחזוקה של AF
בהקשר זה, בחולים עם מחלת עורקים כליליים, קיימות שלוש אפשרויות לשינויים בשריר הלב הפרוזדורי.
1. המודינמי - עומס יתר של הפרוזדורים LA או שניהם.
2. אריתמי - הפרה של אוטומטיזם, מוליכות, ריגוש.
זה תלוי בטקטיקות הטיפול ב-AF.
קבוצה 1 - כוללת את ההתקף הראשון, הן הושלמה באופן ספונטני והן דורשת היפוך תרופתי או חשמלי.
קבוצה 2 - AF חוזרת בחולים לא מטופלים; כולל 3 תת קבוצות:
התקפים אסימפטומטיים שזוהו במקרה במהלך מחקר א.ק.ג. או ניטור דופק 24 שעות ביממה;
נדיר, מתרחש לא יותר מפעם אחת ב-3 חודשים;
תכופות - יותר מהתקף אחד כל 3 חודשים.
קבוצה 3- כוללת התקפים חוזרים ונשנים של AF בחולים המתפתחים למרות נטילת תרופות אנטי-ריתמיות למניעת התקפים (בפרט, חוסמי תעלות Na ו-K); מורכב משלוש תת קבוצות:
פחות מ-3 התקפים ל-3 חודשים בממוצע
בממוצע, יותר מ-3 התקפות ל-3 חודשים.
בדיקה אבחנתית (מינימום) של מטופל עם PFFP
1.1. זיהוי נוכחות וסוג התסמינים
1.2. הגדרה של הסוג הקליני של AF: התקפי, כרוני או לאחרונה
1.3. קביעת שעת ההתקפה הראשונה
1.4. קביעת תדירות, משך, גורמים מעוררים, סוג הקלה בהפרעות קצב
1.5. זיהוי מחלות לב וגורמים אפשריים אחרים ל-AF
2. אלקטרוקרדיוגרמה (ECG)
2.1. היפרטרופיה של חדר שמאל
2.2. משך וצורתו של גל P בקצב הסינוס
2.3. זיהוי שינויים בריפולריזציה, חסימות, סימנים של אוטם שריר הלב ואנומליות אחרות
2.4. נוכחות של תסמונות קדם-עירור חדריות, חולשת קשרי סינוס, ריפולריזציה מוקדמת ומרווח QT ארוך
3. אקו לב (EchoCG)
3.1. איתור פתולוגיה של הלב
3.2. מידות של אטריום שמאל וחדרים אחרים של הלב
3.3. מצב מנגנון המסתם של הלב, הערכת מידת הרגורגיטציה
3.4. דרגת היפרטרופיה של חדר שמאל
3.5. הערכת אינדיקטורים לתפקוד ההתכווצות של החדר השמאלי
3.6 בדיקת מצב קרום הלב
3.7. אבחון של פקקים תוך-חלליים (אפשר רק עם אקו לב טרנס-וושט).
4. קביעת תפקוד בלוטת התריס
5. היעילות והסבילות של AARP ב-AF בעבר לפי האנמנזה.
טיפול תרופתי עבור PFPP.
בתחילת הטיפול ב-PFFP יש לזכור שלראשונה בחיים יש להפסיק את הפרוקסיזם שנוצר בבית חולים, מאחר והשפעתו על CHD אינה ידועה. עם הישנות תכופות, עצירה ספונטנית, אי שינוי ב-CHD ומצבו הכללי של החולה - אין טעם לעצור כל התקף - יש צורך לעסוק במניעה. זה כבר לא ראוי להילחם על החזרת קצב הסינוס בכל מחיר עם קרדיומגליה חמורה, הפרעות הולכה AV עם קצב נדיר של התכווצויות חדריות. בחולים עם SSSU, בשל הסיכון הגבוה לעצירת צומת הסינוס בהשפעת תרופות אנטי-ריתמיות, מוצע IVR.
סיווג תרופות נגד הפרעות קצב (Vaughan Williams E.M.)
תרופות המעכבות הולכה מתווכות באמצעות תעלות נתרן מהירות.
Ia האטה של שלב 0 של דה-פולריזציה של הממברנה. התנהגות עיכוב. הארכת הקיטוב מחדש
Ib השפעה מינימלית על שלב 0 בקרדיומיוציטים נורמליים ודיכוי שלב 0 בנגע תהליך פתולוגי. קיצור של ריפולריזציה.
Ic עיכוב מובהק של שלב 0. עיכוב מובהק בהולכה. השפעה חלשה על קיטוב מחדש.
מחלקה II. חוסמי בטא
תרופות מסוג III שמאריכות את הקוטב מחדש.
אנטגוניסטים לסידן Class IV.
להקלה על AF, נעשה שימוש מסורתי ב-AARP של הקבוצה הראשונה לפי הסיווג של E.M.Vaughan Williams / 84 /. היעילות של rhythmylene, quinidine, novocainamide היא בערך זהה. השימוש בתרופות אלו אינו רצוי בהפרעות ההולכה הראשוניות ועל רקע SSS. אפקט וגוליטי של תרופות 1 גרם. יכול להוביל להתרחשות של רפרוף פרוזדורים עם יחס הולכה של 1: 1, סוג טכיקרדיה חדרית, פירואט,. יש לקחת בחשבון את ההשפעה הקרדיו-דיכאונית שלהם בחולים עם תפקוד לקוי של התכווצות שריר הלב, עם AMI. תרופות אלו מתבטלות כאשר ה-QRS מתרחב ביותר מ-50%, או שה-int מתארך. QT יותר מ-25%.
בעבר, תרופת הייחוס 1 גרם. ת. צורת השחרור הממושכת המודרנית היא קינידין-durules. לעתים קרובות נעשה שימוש במשטר של 1400 מ"ג ליום, 200 מ"ג עם מרווח של שעתיים. מינון ניסוי של 100 מ"ג ניתן מראש. חלק מהכותבים השיגו שחזור של קצב הסינוס ב-95% מהחולים. ברוב המקרים, הקלה ב-AF מתרחשת ביום הראשון לטיפול. בעבר, נעשה שימוש במינון של 2400 מ"ג לשנייה. בעת ניטור, ניתן להבחין בקצב מעבר - אפיזודות של רפרוף פרוזדורים, קצב צומת, קצב סינוס כלילי. במקרה זה, כינידין אינו מבוטל. AF משתנה לקצב הסינוס עם HR של 1 דקה. ברדיקרדיה עשויה להיות הסימן הראשון ל-SSSU. תופעות לוואי - בחילות, הקאות, שלשולים, ירידה בלחץ הדם /, כינידין, התעלפות /. בחולים קשישים, כמו גם באלה עם CHF - עקב ירידה בפינוי של כינידין - ירידה ב מנה יומיתב-25%.
היכולת של התרופה להאריך int. QT יכול להוביל מוקדם אקסטרסיסטולה חדרית, סיכון מוגבר ל-PVT מסוג "פירואט". סוג זה של הפרעת קצב יכול להיות קטלני. טיפול חירום - החדרת תמיסה של 25% מגנזיום גופרתי 2-4 גרם. למשך 1-2 דקות. או EX חיצוני עד ביטול הכינידין להאטת קצב הלב משולבים כינידין עם איזופטין או עם BAB. השילוב של כינידין עם גליקוזידים לבביים מגביר את הסיכון להרעלת גליקוזידים, במיוחד בחולים קשישים. פנוברביטל מפחית את פעילות הכינידין.
משמש לעתים קרובות תוך ורידי להקלה על AF לא מסובך, הכרחי לטיפול חירום. בדרך כלל ניתן עד 10.0 מ"ל / 1 גרם / ON כל 20 דקות, אך לא יותר מ-2.5 גרם. עם ניטור מתמיד של לחץ הדם, קצב הלב והאקג. מתן ראשוני של 10 מ"ג רלניום מגביר את פעולת NA / Zaitsev OG, 1988 / בזמן שחזור קצב הסינוס, מתן התרופה מופסק. בקשר לאפשרות של הפחתת לחץ דם, הוא מנוהל במצב אופקי של המטופל, עם מזרק מוכן עם 0.1 מ"ג של פנילפרין (מזטון).
תופעות הלוואי כוללות: אפקט אריתמוגני, הפרעות קצב חדריות עקב הארכת מרווח ה-QT; האטה של הולכה אטרי-חדרי, הולכה תוך-חדרית (הם מתרחשים לעתים קרובות יותר בשריר הלב הפגוע, מופיעים ב-ECG כהרחבת קומפלקס החדרים וחסימה של הרגליים של צרור His); תת לחץ דם עורקי (עקב ירידה בעוצמת התכווצויות הלב ואפקט הרחבת כלי הדם); סחרחורת, חולשה, פגיעה בהכרה, דיכאון, דליריום, הזיות; תגובות אלרגיות.
התוויות נגד לשימוש ב-NA הן: תת לחץ דם עורקי, הלם קרדיוגני, אי ספיקת לב כרונית; sinoatrial ו-AV block II ו-III דרגה, הפרעות הולכה תוך חדרית; הארכה של מרווח ה-QT ואינדיקציות לאפיזודות של טכיקרדיה פירואטית בהיסטוריה; אי ספיקת כליות חמורה; זאבת אדמנתית מערכתית; רגישות יתר לתרופה.
עם לחץ דם נמוך תחילה, נאסף מיקרוגרם של mezaton (פנילפרין) במזרק אחד עם NA. בחולים מבוגרים, שילוב זה יכול לגרום לעלייה חדה בלחץ הדם ואף להתקף של ALHF. לכן, רצוי להפחית את מינון של NA.
ההשפעה הרעילה של נובוקיינמיד מסולקת על ידי הזרקה תוך ורידית של 100 מ"ל של תמיסה 5% של נתרן ביקרבונט.
מוכנס פנימה / ורידי באמצעות סילון למשך 5 דקות. במידת הצורך, חזור על החדרת מ"ג לאחר שעתיים. AF נעצר כל דקה עד 60% מהמטופלים.
כאשר נלקח דרך הפה, מנה בודדת, המינון היומי הממוצע.
1. כיווץ כלי דם, התנגדות כלי דם היקפית מוגברת, הגברת DBP ב-5-20 מ"מ ובכן.
2. אפקט אינוטרופי שלילי, התרחשות או עלייה בתסמיני CHF בחולים עם הפרעה בתפקוד החדר השמאלי.
3. פעולה אנטיכולינרגית - יובש בפה, הפרעות באקוורציה חזותית, עצירות, אצירת שתן חריפה.
4. האטה בהולכה AV.
סיבוכים נדירים - פסיכוזה חריפה, צהבת כולסטטית, היפוגליקמיה.
1. סינוס ברדיקרדיה, כולל SSSU.
2. הפרה של הולכה תוך-חדרית ו-AV.
3. אי ספיקת לב חמורה.
בהתאם להמלצות איגוד הלב האמריקני והאיגוד האירופאי לקרדיולוגיה / 2001 / תרופות 1 ,C, class /etacizin, propafenone/ הם הקו הראשון לטיפול ב-AF בהיעדר מחלת לב אורגנית. R.N. Forogos מאמין שלתרופות אלו יש את האיזון הטוב ביותר בין יעילות ובטיחות בקבוצת חולים זו.
מעכב תהליך שחזור תעלות נתרן מהירות של ממברנת הקרדיומיוציטים, מעכב חלקית את זרם הסידן הנכנס האיטי. מאריך את מרווח ה-P-R, מרחיב את קומפלקס QRS בהתאם למינון. אינו משנה את מרווח QT, לחץ דם ראשוני. נספג במהירות ממערכת העיכול, נקבע בדם לאחר 30-60
דקות, מגיע לריכוז מקסימלי לאחר 3 שעות. מנה בודדת של 100 מ"ג אתציזין משחזרת את קצב הסינוס ב-AF ברוב החולים. . התרופה אינה משפיעה על קצב הלב אפילו בחולים עם ברדיקרדיה חמורה / למעט SSSU /. לא מומלץ לשימוש עם חסימת SA, חסימת A-B של 2-3 מעלות, חסימת רגלי ה-His, CHF (עם EF פחות מ-40%), פגיעה בתפקוד הכבד והכליות. Etatsizin משולב עם קורדרון, דיגוקסין ו-BAB. חומצה גלוטמית מנטרלת את ההשפעה הקרדיו-דיכאונית של אטציזין.
במחקרים מבוקרי פלצבו, פרופנון תוך ורידי משחזר את קצב הסינוס בתוך שעות בכ-81% מהחולים ( Nacarelli GV, Dorian P, Hohnloser SH. ועוד)
ניתן להשתמש במנה בודדת של ריתמונורם דרך הפה כדי לעצור AF מתמשך מחוץ לבית החולים / , גלולה בכיס, / .
בבית חולים היא ניתנת לווריד במינון של 1-2 מ"ג/ק"ג משקל גוף בתמיסת גלוקוז של 5% למשך דקה. יש ליטול תחילה חוסם בטא או AK non-dihydroperidine כדי למנוע הולכה מהירה דרך צומת AV, התחלה של רפרוף פרוזדורים עם קצב חדרים גבוה.
ל-BAB יש פעילות אנטי-אריתמית מתונה למדי, לפיכך, היעילות של obzidan היא עד 8% / I.P. זמוטאייב, 1985 / לעיתים קרובות יותר יש האטה במספר התכווצויות החדרים עקב עיכוב הולכת AV, המשמשת בפועל.
מחלקה III. קורדרון
השימוש בקורדרון נחשב לטקטיקה סבירה להפיכה תרופתית של AF - רמת הראיות A. שונה לטובה מרוב ה-AAPs האחרים על ידי האפשרות להשתמש בו בחולים עם תסמונת SVC וב-CHF, למעט קרדיומגליה. Cordarone היא תרופת הבחירה בטיפול ב-AF בחולים עם מחלת לב אורגנית / Smetnev A.S. 1990, Zipes D.P. 2000 / ניתן בתחילה לווריד במינון של 5-7 מ"ג/ק"ג משקל גוף, למשך דקות. לאחר מכן חזור על ההקדמה של 1.2-1.8 גרם ליום או במתן פומי במספר מנות עד שמגיעים למינון כולל של 10 גרם. מנת תחזוקה נוספת/יום. ירידה קצרת טווח בלחץ הדם אפשרית - ורק עם הפעלה מהירה מאוד/בקדמה - עקב ירידה ב-OPSS, המלווה בעלייה מסוימת בקצב הלב ובעלייה בתפוקת הלב.
בבית החולים, תוכניות אחרות אפשריות: המינון הראשוני הוא 1.2-1.8 גרם ליום במספר מנות עד למינון כולל של 10 גרם. לאחר מכן מנת תחזוקה / יום. קרדיוורסיה מתרחשת בדרך כלל בימים הראשונים של הטיפול.
תור לאישפוז גרם ליום עד 10 גרם. רוויה. לאחר מכן מנת תחזוקה / יום.
עם עלייה במשך ההתקף, השפעת הקורדרון פוחתת. חשוב שהתרופה תהיה יעילה ב-AF עמיד לטיפול עם AAP/Shamov I.A אחרים. .89 /. ההשפעה הפרעת קצב קטנה מזו של AAPs אחרים - בערך 1-5% מהחולים. על א.ק.ג. התארכות int אפשרית. QT, הופעת טכי-קצב חדריות, כולל סוג ה"פירואטה".
אינטראקציה של קורדרון עם תרופות אחרות:
a/ BAB, ACC - יתר לחץ דם, ברדיקרדיה,
b/ לידוקאין - ברדיקרדיה,
c/ disopyramide - סיכון להפרעות קצב חדשות,
d/ fentanyl - תת לחץ דם, ברדיקרדיה, ירידה ב-CO,
e/ rifampicin - ירידה בריכוז הקורדרון. .
Class IV / verapamil, diltiazem /
Verapamil בחולים עם AF בהיעדר מסלולים נוספים משמש להפחתת קצב הלב / המלצה בדרגה 1 / .
השפעת ההקלה היא בדרך כלל מתונה - עד 20% מהמקרים. התווית נגד ב-SVC, tk. במצב זה מעלה את תדירות ההתכווצויות של החדרים ל-300 בדקה אחת. עד פרפור חדרים. זה ניתן במינון של 0.075-0.15 מ"ג לק"ג משקל גוף למשך 2 דקות. , תחילת הפעולה בעוד 3-5 דקות.
טבלה 2. מינונים ממוצעים של AARP במתן תוך ורידי
אם PFFP מתרחש לפני 48 שעות, בפעם הראשונה או שוב ושוב, ומלווה בטכיקרדיה חמורה, הפרעה מתונה ב-CHD, נסבל באופן סובייקטיבי גרוע על ידי המטופל, תרופה אנטי-ריתמית ניתנת באופן פרנטרלי. אם תרופה אחת נגד הפרעות קצב נכשלת, הטיפול התרופתי בשלב הטרום-אשפוזי מופסק.
התוויות נגד לשיקום קצב הסינוס בשלב הטרום-אשפוזי:
משך AF הוא יותר מיומיים.
הרחבה מוכחת של אטריום שמאל (גודל קדמי-אחורי 4.5 ס"מ לפי אקו לב).
נוכחות של קרישי דם בפרוזדורים או היסטוריה של סיבוכים תרומבואמבוליים.
התפתחות הפרוקסיזם על רקע חריף תסמונת כלילית(בנוכחות המודינמיקה יציבה).
התפתחות של הפרוקסיזם על רקע הפרעות אלקטרוליטים חמורות.
אינדיקציות לאשפוז.
a/ FP שנרשם לראשונה.
ב/ התקפיות ממושכת,
ג / חוסר השפעה מטיפול תרופתי,
d/ התקפיות עם תדירות גבוהה של התכווצויות חדריות והתפתחות של סיבוכי הפרעות קצב,
e/ הישנות תכופות של AF (לבחירת טיפול אנטי-ריתמי). .
חולים עם PFFP יותר מ-48 שעות עם סבילות טובה, ללא הפרה של CHD למשך שלושה שבועות, רושמים וורפרין. INR נשלט פעם בשבוע, בטווח של 2.0-3.0. יש לזכור כי בערכים של INR פחות מ-2, היעילות של מניעת שבץ איסכמי מופחתת. בעזרת BAB קצב הלב נשלט. לאחר תגובה שלילית לאקו לב טרנס-וושט של התוספתן LA, נקבעת קרדיווסיה דרך הפה.
1. בצעו מיידית קרדיוורסיה חשמלית בחולים עם AF התקפי וקצב חדריות מהיר, אלו עם עדות ECG של MI חריף או תת לחץ דם סימפטומטי, אנגינה פקטוריס או CLE אם AF לא מגיבה מיד לאמצעים תרופתיים. (רמת ראיות: ג)
2. בצע היפוך חילופין בחולים ללא חוסר יציבות המודינמית כאשר תסמיני AF אינם מקובלים. (רמת ראיות: ג)
1. קרדיוורסיה פרמקולוגית או חשמלית להאצת חזרה ספונטנית לקצב הסינוס בחולים עם אפיזודה חדשה של AF. (רמת ראיות: ג)
2. קרדיוורסיה חשמלית בחולים עם AF מתמשך אם הישנות מוקדם אינה סבירה. (רמת ראיות: ג)
3. גירסה חוזרת של הלב לאחר טיפול מניעתי בחולים שחזרו ל-AF ללא טיפול אנטי-ריתמי לאחר היפוך לב מוצלח. (רמת ראיות: ג)
1. הסבה תרופתית לקצב סינוס בחולים עם AF מתמשך. (רמת ראיות: ג)
2. מתן מחוץ לבית חולים של תרופות תרופתיות ל-Cdioversion של AF שאובחן לאחרונה, התקפי או מתמשך בחולים ללא מחלת לב, או כאשר בטיחות התרופה נבדקה בחולה זה. (רמת ראיות: ג)
1. קרדיוורסיה חשמלית בחולים עם החלפה ספונטנית של AF וקצב סינוס לפרקי זמן קצרים. (רמת ראיות: ג)
2. חזור על קרדיוורסיה בחולים עם תקופות קצרות של קצב סינוס שחוזרים ל-AF למרות ריבוי הליכי הלבבות וטיפול אנטי-אריתמי מונע. (רמת ראיות: ג)
לכן, בצורת הפראוקסיזמלית של AF, זה צריך להיחשב חשוב ביותר להפסיק במהירות - תוך 1-2 ימים - את ההתקף הראשון של AF בחייו של המטופל, במיוחד בפתולוגיה חמורה של שריר הלב.
אסור להפסיק לפני השימוש המהיר בטיפול בדחפים חשמליים (EIT) בחולים כאלה, מבלי לבזבז זמן על ניסיונות ארוכי טווח להחזיר את הקצב באמצעות תרופות, הכרוכות בעלייה באיום של פקקת תוך לבבית חריפה (ובהמשך. תרומבואמבוליזם, כולל "נורמליזציה"). במקרה של LT עם קצב חדרי תכוף (כאשר מבצעים 2:1, במיוחד 1:1), גם היפוך מיידי מוצדק ביותר.
סוכנים פחות יעילים או לא נלמדים
בחולים עם AMI, או בנוכחות ברדיקרדיה, הפרות חדות CHD - OLZHN, ירידה בלחץ הדם, - תרופות אנטי-אריתמיות יכולות להראות אפקט פרו-אריתמי וקרדיודיכאוני. השיטה הטובה ביותר היא EIT.
עם טכי-קצב משמעותי, תדירות התכווצויות החדרים היא 200 או יותר בדקה אחת,
קיים סיכון גבוה לפרפור חדרים. נדרש EIT.
1. בצע היפוך חשמל בחולים עם פגיעה המודינמית חמורה או איסכמיה חמורה. (רמת ראיות: ג)
2. מתן תוך ורידי של גליקוזידים לבביים או אמיודרון להאטת התגובה המהירה של החדרים ולשיפור תפקוד LV. (רמת ראיות: ג)
3. מתן תוך ורידיחוסמי בטא להאטת התגובה המהירה של חדרי הלב בחולים ללא הפרעות בתפקוד LV קליני, מחלה ברונכוספסטית או חסימת AV. (רמת ראיות: ג)
4. תן הפרין לחולים עם AF ו-MI חריף, אלא אם כן התווית נגד קרישה. (רמת ראיות: ג)
1. אבלציה של צנתר מסלול אביזר בחולים סימפטומטיים עם AF שיש להם תסמונת WPW, במיוחד אלו עם סינקופה עקב קצב לב מהיר או תקופה קצרה של DPP. (רמת ראיות: ב)
2. בצעו מיידית קרדיוורסיה חשמלית למניעת פרפור חדרים בחולים עם WPW שיש להם AF עם תגובה חדרית מהירה הקשורה לאי יציבות המודינמית. (רמת ראיות: ב)
3. לתת פרוקאינאמיד או איבוטיליד תוך ורידי כדי להחזיר את קצב הסינוס בחולים עם WPW שיש להם AF ללא אי יציבות המודינמית ברחבה מתחמי QRSעל הקרדיוגרמה (גדול מ-120 אלפיות השנייה או שווה ל-120 אלפיות השנייה). (רמת ראיות: ג)
מתן תוך ורידי של quinidine, procainamide, disopyramide, ibutilide או amiodarone לחולים יציבים המודינמית עם AF הכוללים מסלולים נלווים. (רמת ראיות: ב)
1. נדרשת חילוף חומרים מיידי אם מתפתחת טכיקרדיה או אי יציבות המודינמית בתדירות גבוהה מאוד בחולים עם AF הכולל מסלול עזר. (רמת ראיות: ב)
מתן תוך ורידי של חוסמי בטא, גליקוזידים לבביים, דילטיאזם או ורפמיל בחולים עם תסמונת WPW שיש להם פרה-אקסיטציה חדרית ב-AF (רמת ראיות: B)
1. נדרשת חילוף חומרים מיידי אם מתפתחת טכיקרדיה או אי יציבות המודינמית בתדירות גבוהה מאוד בחולים עם AF הכולל מסלול עזר. (רמת ראיות: ב)
1. תן חוסמי בטא לפי הצורך כדי לשלוט בשיעור התגובה של חדרי הלב בחולים עם AF מסובך על ידי תירוטוקסיקוזיס, אלא אם כן התווית נגד. (רמת ראיות: ב)
2. בנסיבות שבהן לא ניתן להשתמש בחוסמי בטא, יש לתת אנטגוניסטים לסידן (דילטיאזם או ורפמיל) כדי לשלוט בקצב התגובה של החדרים. (רמת ראיות: ב)
3. בחולים עם AF הקשורים ל-thyrotoxicosis, השתמשו בנוגדי קרישה דרך הפה (INR 2-3) למניעת תרומבואמבוליזם, כפי שהומלץ לחולי AF עם גורמי סיכון אחרים לשבץ מוחי. (רמת ראיות: ג)
א. לאחר שמצב בלוטת התריס משוחזר, ההמלצות לטיפול מונע אנטי-טרומבוטי נשארות זהות לאלו של חולים ללא יתר פעילות בלוטת התריס. (רמת ראיות: ג)
לטפל בחולים עם קרדיומיופתיה היפרטרופית המפתחים AF עם נוגדי קרישה דרך הפה (INR 2-3) כפי שהומלץ לחולים אחרים בסיכון גבוה כדי למנוע תרומבואמבוליזם. (רמת ראיות: ב)
מתן תרופות אנטי-אריתמיות כדי למנוע הישנות של AF. הנתונים הזמינים אינם מספיקים כדי להמליץ על חומר יחיד בהגדרה זו, אך בדרך כלל מועדפים דיסופרמיד ואמיודרון. (רמת ראיות: ג)
עם AF תלוי מגנזיום (היפומגנזמיה מוכחת או נוכחות של מרווח QT ממושך), תרופת הבחירה היא קורמגנזין (מגנזיום סולפט), שבמקרים אחרים מהווה אמצעי נוסף להאטת הקצב. ניתן ב/in למשך דקות. במינונים של מגנזיום (מ"ל 10% או מ"ל 20% תמיסה).
טיפול ב-PFFP חוזר.
עבור PFFPs קצר עם סימפטומים מינימליים, סביר שלא להשתמש בטיפול אנטי-אריתמי. זה נדרש בדרך כלל אם הופעת AF מלווה בתסמינים חמורים. בשני המצבים, יש צורך באמצעים כדי לשלוט בקצב הלב ולמנוע סיבוכים תרומבואמבוליים. בחולים רבים, תרופות שונות נגד הפרעות קצב עשויות להיות יעילות, והבחירה הראשונית בתרופה צריכה להתבסס על שיקולי בטיחות. יש להדגיש כי נתונים מניסויים אקראיים של תרופות אנטי-ריתמיות ב-AF הם נדירים, המלצות לבחירת תרופה מסוימת מבוססות בעיקר על הסכמת מומחים ועשויות להשתנות ככל שעובדות חדשות יהיו זמינות.
אפקט פרו-אריתמי של AARP.
מחקר וניסיון קליני מראים כי השפעות פרו-ריתמיות מסכנות חיים מתרחשות בכ-10% מהמקרים עם טיפול אריתמי ארוך טווח. במקרה זה, ההשפעה הפרה-ריתמית מתבטאת בהתחלת הפרעת קצב חדשה שטרם נצפתה אצל מטופל זה. במקרים מסוימים מתפתחים אפילו הבהוב ורפרוף של חדרי הלב. לכן, השפעות אנטי-ריתמיות או הפרעות קצב עלולות לגרום לאיום מיידי על חיי המטופל. המסקנה המעשית עבורנו הרופאים היא שמטופלים הנוטלים תרופות אנטי-ריתמיות לאורך זמן דורשים מעקב ובקרה מתמידים וקפדניים.
הסיכון גבוה במיוחד עבור חולים שכבר יש להם מחלות לב וכלי דם. אלה כוללים חולים עם חלק פליטה נמוך, אי ספיקת לב, CAD מתקדם או קרדיומיופתיה. קבוצת הסיכון כוללת גם חולים עם הפרעות מטבוליזם של אלקטרוליטיםאו אנשים שצורכים אלכוהול על בסיס קבוע.
נכון, ההשפעות הפרו-קצביות של AARP אינן תמיד מסכנות חיים. לעיתים הם מתבטאים באקסטרה-סיסטולות מתונות או בהפרעות הולכה.
טבלה 5. סוגי הפרעות קצב וחסימות הולכה במהלך טיפול ב-AF עם AAs שונים לפי סיווג Vaughan Williams.
ב. הפרעות קצב פרוזדוריות
ב.הפרות של הולכה ויצירת דחפים
טבלה 6. רשימת תרופות בעלות פוטנציאל פרו-אריתמי
מניעת תרומבואמבוליזם ומתן נוגדי קרישה. כאשר קצב הסינוס משוחזר.
שחזור קצב הסינוס בחולים עם AF עשוי להיות מלווה באמבוליזציה מערכתית ב-1-3% מהמקרים. אמבוליזציה עשויה להתרחש ימים או אפילו שבועות לאחר המרת קרדיו מוצלחת. בהקשר זה, במהלך הליך זה, טיפול ב-OAC מומלץ למשך 3 שבועות לפני ו-4 שבועות לאחר היפוך לב. במקרים בהם לא ניתן לשחזר את קצב הסינוס, משך הטיפול ב-OAC נקבע לפי הגיל ונוכחות גורמי סיכון. במקרה של AF חריפה (72 שעות), התגלו פקקים תוך-לביים ב-14% מהחולים. לכן, יש לרשום לכל חולים כאלה הפרין למשך 48 שעות. אם במהלך תקופה זו לא ניתן היה לשחזר את קצב הסינוס, והתקבלה החלטה על קרדיו-version, יש צורך להתחיל בטיפול OAC. אם מתגלים קרישי דם באטריום בחולים עם AF, עם היסטוריה של תסחיף מערכתי, הטיפול ב-OAC ממשיך לכל החיים. הדבר נכון גם למטופלים עם תותבות מסתמים מכניות, הרמה הרציונלית של INR היא 4.0.
הסיכון לסיבוכים תסחיפים ב-AF לא ראומטי גבוה פי 5.6 מאשר בקבוצת הביקורת, וב-AF ראומטי הוא גבוה פי 17.6. הסיכון הכולל לסיבוכים תסחיפים גבוה פי 7 כאשר AF קיים.% מכל השבץ האיסכמי מתרחש עם AF. הבדלים משמעותיים בסיכון לסיבוכים תסחיפים ב- paroxysmal or צורות כרוניותלא, למרות שכמה מחברים מציינים ש-AF כרוני נושא כמה סיכון גדול יותר(6% לשנה) מאשר פרוקסימלי (2 - 3% בשנה).
הסיכון הגבוה ביותר לסיבוכים תסחיפים ב-AF הוא במצבים הבאים:
א/ התחילה לאחרונה AF,
ב/ השנה הראשונה לקיומו של ה-FI,
בתקופה הקרובה ביותר לאחר שחזור קצב הסינוס.
הסיכון לשבץ ב-AF עולה עם הגיל, כמו קבוצת גילמגיל 50 עד 59 שנים, 6.7% מכלל המקרים של כלי דם במוח קשורים ל-AF, ובקבוצת הגיל שבין 80 ל-89 שנים - 36.2%.
טיפול נוגד קרישה הוא האסטרטגיה העיקרית למניעת סיבוכים תסחיפים. זה מפחית את הסיכון שלהם בממוצע של 68%, אבל קשור לסיכון לדימום רציני (כ-1% בשנה). ב-AF לא ראומטי, הפשרה האופטימלית בין יעילות לסיכון לדימום היא שמירה על INR של 2-3 (אינדקס פרוטרומבין). היבט נוסף של מניעת סיבוכים תסחיפים הוא שיקום ושמירה על קצב הסינוס. עם זאת, מחקרים ארגוניים רב-מרכזיים שהעריכו את יחס הסיכון/תועלת (במיוחד עבור הסיכון של טיפול אנטי-ריתמי אחזקה) לא הושלמו.
עם משך AF יותר מ-48 שעות, נוגדי קרישה דרך הפה (OAC) מסומנים לפחות 3 שבועות לפני (אפשרי אשפוז חוץ) וחודש אחד לאחר שחזור קצב הסינוס. המינון הראשוני של OAC נבחר תוך התחשבות במצב התפקודי של הכבד, מחלות נלוותוהטיפול שלהם, מדד INR. הנפוץ ביותר בעולם הוא נגזרת של מונוקומרין - וורפרין - בשל משך פעולתו האופטימלי וסבילות טובה. זמן מחצית החיים של וורפרין (36 שעות) מספק היפוקואגולציה יציבה, שאינה מאפשרת תנודות בירידה ברמת הפקטור Y11. טען מינונים OAC אינו מומלץ בגלל האיום של פקקת ודימום (על רקע הפרין). יש להתחיל בטיפול במינוני תחזוקה של וורפרין - 2.5-10 מ"ג ליום.
במקביל (במקביל), נעשה שימוש בהפרין בשליטה של APTT למשך 5 ימים, ולאחר מכן בוטלה האחרון. יש צורך לדעת כי צפלוספורינים מעכבים את היווצרות ויטמין K2 חיידקי מעייםולחסום את מחזור ויטמין K. מאחר ש-OAC עובר חילוף חומרים בכבד על ידי מערכת הציטוכרום P 450, יש צורך לקחת בחשבון את השפעת התרופות על מערכת CR 450. עם עמידות גנטית ל-OAC, אפילו עלייה של פי 20 במינון המרבי של התרופה אינו גורם להיפוקרישה. אינדיקטור INR מומלץ להישמר בטווח של 2.0-3.5, ובאנשים מעל גיל 75, לא יותר מ-3.0. חריגה של INR מעל 3.0 מגבירה את הסיכון לדימום תוך גולגולתי אצל אנשים מעל גיל 75 עד ל-1.9% מהמקרים.
אקו לב טרנס-וושט (PE ECHO) היא שיטה רגישה ביותר לזיהוי פקקים פרוזדורים שמאליים (LA), אולם ישנם דיווחים על מקרים של תסחיף ב-AF בהיעדר פקקת LA שזוהתה על ידי PE ECHO. עם זאת, מוצעת האסטרטגיה הבאה:
- אם AF קיים במשך יותר מ-48 שעות, ובמקרה של ECHO חירום (מיד לפני המחקר, בהכרח ניתנים הפרין), לא מתגלים פקקות LA, אז מבוצעת היפוך קרדיו מיידית (תרופתית או חשמלית).
- אם טרומבי LA מתגלים במהלך PE ECHO, נוגדי קרישה נקבעים למשך 6 שבועות ו-PE ECHO חוזר על עצמו (מספר פעמים), ולאחר מכן ...
- אם טרומבים מתמוססים (הם אינם מזוהים עוד במהלך ECHO חירום), אזי מבוצעת קרדיוורסיה חשמלית, ואם הם לא מתמוססים, אזי זו התווית נגד לקרדיוהורסיה.
1. התחל טיפול אנטי-תרומבוטי (נוגד קרישה דרך הפה או אספירין) בכל החולים עם AF, למעט חולים עם AF בודד, למניעת תרומבואמבוליזם. (רמת ראיות: א)
2. התאמה אישית של בחירת התרופה האנטי-טרומבוטית, בהתבסס על הערכה של הסיכון המוחלט לשבץ ולדימום, וכן על יחס הסיכון-תועלת לכל מטופל. (רמת ראיות: א)
3. טיפול נוגד קרישה פומי כרוני במינון מותאם להשגת INR של 2-3 בחולים בסיכון גבוה לשבץ מוחי, אלא אם כן התווית נגד. (רמת ראיות: א)
א. יש להעריך מחדש באופן קבוע את הצורך בנוגדי קרישה. (רמת ראיות: א)
ב. יש למדוד את ה-INR לפחות שבועי במהלך התחלת נוגדי קרישה וחודשי כאשר החולה יציב. (רמת ראיות: א)
4. לתת אספירין 325 מ"ג מדי יום כחלופה בחולים בסיכון נמוך או בחולים עם התוויות נגד לנוגדי קרישה דרך הפה. (רמת ראיות: א)
5. לתת נוגדי קרישה דרך הפה לחולים עם AF שיש להם מחלת מסתם מיטרלי ראומטי או מסתמי לב תותבים (מכניים או רקמות). (רמת ראיות: ב)
הגדר את עוצמת היעד של נוגד קרישה בהתאם לסוג התותב, אך לא פחות מ- INR 2 - 3. (רמת ראיות: B)
טבלה 7 טיפול אנטי-טרומבוטי מבוסס על רמת הסיכון בחולים עם AF
גורמי סיכון לתרומבואמבוליזם: HNK, חלק פליטת LV פחות מ-35% והיסטוריה של יתר לחץ דם.
עמידות AF לטיפול תרופתי.
מהי ההתנגדות ל-AARP, מהם המנגנונים שלה? חוסר רגישות ראשונית לתרופה עשויה להיות קשורה לאופי ולחומרתה של המחלה הבסיסית. ניסיונות לקשר את היעילות של תרופה אנטי-ריתמית כזו או אחרת עם האטיולוגיה של הפרעות קצב לב בספרות אינם בודדים. עם זאת, נושא זה דורש מחקר נוסף, מכיוון שהנתונים של מחברים שונים סותרים מאוד (אנטונצ'נקו I.V., Savenkova G.M., Popov S.V.)
טיפול אנטי-אריתמי פחות יעיל לשינויים אורגניים גדולים בשריר הלב. הוכח כי מנבאים בלתי תלויים של עמידה ב-AF לטיפול תרופתי הם: ירידה בפרק הפליטה, מפרצת חדר שמאל, אי ספיקת מסתם אבי העורקים במקביל. שמירה על קצב הסינוס קשה משמעותית עם גדלים גדולים (או נפח) של אטריום שמאל (LA) [. קושקובסקי מ.ס. לשצ'ינסקי L.A., Tyulkina E.E.) עם זאת, לגבי קורדרון, לא נמצא מתאם ברור בין יעילות התרופה לגודל ה-LA [. אברם ר., קריסטודורסקו ר) . בארט ב.יה. ומחברים מציינים שקשר כזה לא נוצר בחולים עם תוצאה חיוביתטיפול, אך ב-71% מהחולים ללא השפעה מנטילת קורדרון, גודל ה-LA עלה על 5.5 ס"מ. Antonchenko et al. הוכח כי עלייה בדרגת הפיברוזיס באטריום השמאלי המורחב בחולים עם AF מלווה גם בירידה ביעילות של טיפול מונע ארוך טווח. קיימות אינדיקציות לעמידות לטיפול ב-AF בחולים עם חסימה היפרטרופית קרדיומיופתיה [Bokeria L.A., Borisov K.V.). עם רפרוף פרוזדורי חוזר מתמשך, עמיד לטיפול אנטי-אריתמי מניעתי, התגלו דיברטיקולה ודיספלסיה אריתמוגנית של הפרוזדור הימני במספר חולים צעירים ללא סימנים ברורים של מחלת לב אורגנית [. בוקריה L.A., Revishvili A.Sh., Sveshnikov A.V.)
טיפולים לא תרופתיים עבור AF.
הגירסה חשמלית - פריקה חשמליתזרם ישר, מסונכרן עם פעילות הלב, בדרך כלל על גל R של הקרדיוגרמה. זה מבטיח שגירוי חשמלי לא יתרחש בשלב הפגיע של מחזור הלב: ה-ms לדופק אחרי החלק העליון של גל ה-T. הילוכים חשמליים משמשים לטיפול בכל קצב הלב החריג למעט פרפור חדרים. המונח "דפיברילציה" מרמז על הלם אסינכרוני, הכרחי לטיפול בפרפור חדרים, אך לא AF.
במחקר אחד, 64 מטופלים חולקו אקראית ל-Cdioversion חשמלי עם אנרגיה ראשונית בצורת גל מונופאזית של 100, 200 או 360 J. אנרגיה התחלתית גבוהה הייתה יעילה משמעותית מאנרגיה נמוכה יותר (שיעור ההצלחה המיידי היה 14% ב-100 J, 39% - 200 ו-95% ב-360 J, בהתאמה) וכתוצאה מכך פחות זעזועים ופחות אנרגיה הכוללת כאשר החלה קרדיו-הורסיה ב-360 J. נתונים אלה מצביעים על כך שההלם הראשוני של 100 J לעיתים קרובות נמוך מדי. עבור היפוך חשמלי ב-AF, מומלצת אנרגיה ראשונית של 200 J ומעלה. ישנם מכשירים המייצרים זרם עם צורת גל דו-פאזית; הם משיגים הילוכים ברמות אנרגיה נמוכות יותר מאלו המשתמשות בצורת הגל המונופאזית.
לפיכך, אחוזי ההצלחה ב-Cdioversion חיצוני נע בין 65% ל-90%. הסיכון לקרדיוהורסיה חשמלית נמוך מהסיכון להתקדמות רפואית. סיבוכים נדירים למדי, אך הם מתרחשים ויש צורך להודיע למטופל עליהם בעת קבלת הסכמת המטופל להליך. הסיבוכים העיקריים של קרדיוורסיה חיצונית: תסחיף מערכתי, הפרעות קצב חדריות, סינוס ברדיקרדיה, יתר לחץ דם, בצקת ריאות, גובה מקטע ST. שחזור קצב הסינוס יכול לחשוף תסמונת סינוס חולה או בלוק AV קיים, ולכן בעת ביצוע קרדיוורסיה, יש להיות מוכנים לבצע קצב זמני. התווית קרדיוורסיה חשמלית בהרעלת גליקוזידים לבבית (איחור של שבוע לפחות הגיוני, גם במקרה של צריכה תקינה של גליקוזידים לבביים - ללא שיכרון), היפוקלמיה, זיהומים חריפים ואי ספיקת מחזור לא מפוצה. כיוון שההרדמה החשמלית מצריכה הרדמה כללית, כל התווית נגד להרדמה כללית היא התווית נגד להרדמות חשמלית. על פי כמה תצפיות, היעילות של EIT מגיעה ל-94%. עם זאת, הפרעות קצב חמורות (אסיסטולה חדרית, סינוס ברדיקרדיה, נדידת קוצב לב, הפרעת קצב סינוס), כמו גם סיבוכים אחרים (תרומבואמבוליזם, בצקת ריאות, תת לחץ דם עורקי).
התוויות נגד ל-EIT:
1. הפרוקסיזמים תכופים קצרי טווח של AF, הנפסקים מעצמם או עם תרופות.
2. צורה קבועה של פרפור פרוזדורים:
בן יותר משלוש שנים,
b/ מרשם אינו ידוע.
ד/ תסמונת פרידריך,
e/ שיכרון גליקוזיד,
e/TELA עד שלושה חודשים,
g / תהליך ראומטי פעיל.
קיצוב לב מסומן עבור צורות ברדי וטכי-ברדי של AF (כלומר תסמונת סינוס חולה ובלוק AV). קצב דו-חדרי (DDD, ב-AF paroxysmal) או פרוזדורי (AAI, כולל מחיצה תוך-אטריאלית) עשוי להפחית את שיעורי ההישנות. סוגים שוניםקיצוב (כולל טרנס-וושט) מפסיק לעיתים רחוקות AF.
הקרדיווורטר-דפיברילטור הפרוזדורי המושתל מספק פריקות זרם ישר באנרגיה של _ 6 J, ב דייטים מוקדמים(כמעט מיד) לאחר זיהוי AF. אם לוקחים בחשבון את תופעת השיפוץ האלקטרופיזיולוגי, מעצר מוקדם של AF אינו מאפשר שינויים ברפרקטוריות פרוזדורים, מה שמפחית את התנאים המוקדמים להישנות תכופה ולתחזוקה עצמית של AF. עם זאת, היעילות של שיטה זו ומשמעותה עדיין לא מובנות במלואן.
ניתן לכנות את 20 השנים האחרונות התקופה האלקטרופיזיולוגית בהפרעות קצב קליניות. הודות למחקרים אלקטרופיזיולוגיים, ניתן היה לחקור את הטופוגרפיה של מסלולי ההולכה הנוספים של הלב בחולה מסוים, מה שפתח סיכויים חדשים לטיפול כירורגי בהפרעות קצב. מנתחים-פרעות קצב תרמו תרומה משמעותית להבנת הפתוגנזה של הפרעות קצב לב וגילו עידן חדשבטיפול בפרפור פרוזדורים קשה לטיפול, שלא כונה בטעות "אריתמיה אבסולוטה" קודם לכן. .
עוד בתחילת שנות ה-80, Soh הראה שניתן לטפל בפרפור פרוזדורים באמצעות כמה חתכים בפרוזדורים, ובכך להפריע להתפתחות של מחזור החזרות המרובות הגורמת לפרפור פרוזדורים.
אינדיקציות לטיפול כירורגי ב-AF הן:
א / תסמינים קליניים חמורים;
b/התנגדות לטיפול תרופתי;
ג/ תופעות לוואי.
ד/ היצרות מיטרלי.
שיטות כירורגיות לטיפול ב-AF משמשות כיום לעתים רחוקות. ביניהם, פעולות של בידוד כירורגי של הפרוזדורים, "מסדרון", "מבוך" מובחנים. כולם מכוונים להרס של טבעות כניסה חוזרות מרובות, ויצירת נתיב אחד ("מסדרון", "מבוך") מהאטריה לצומת AV.
הבאים שיטות כירורגיותטיפול AF:
החיסרון העיקרי שלהם הוא שהם מבוצעים על לב "פתוח" (הרדמה כללית, מכונת לב-ריאה, קרדיופלגיה קרה וסיבוכים והשלכות הנובעות מכך). אם יש צורך בניתוח לב פתוח (החלפת מסתם או כריתת מפרצת), ניתן לבצע במקביל ניתוח ל-AF.
שיטות התערבותיות בטיפול ב-AF (אבלציה צנתר באמצעות רדיו-תדרי צנרת) זוכות כיום ליותר ויותר תומכים. השיטה הפשוטה ביותר ל-AF (נפוץ אפילו לפני שנים) היא הרס חיבור ה-AV (יצירת חסימת AV מלאכותית והשתלת קוצב במצב VVI (R). במקרה זה, הפיזיולוגיה של הלב היא מופרע, הסיכון התסחיף אינו פוחת, לעתים קרובות מתרחשת תלות בקוצב הלב וכל החסרונות של מצב VVI. כעת, על מנת לשלוט בתדירות התכווצויות החדרים, מתבצע יותר ויותר שינוי בהולכה AV ללא השתלת קוצב (כלומר , נוצרת הגבלה על הולכת דחפים פרוזדורים לחדרים). פעולות "מבוך").הליך זה יעיל מאוד, אבל מאוד מורכב מבחינה טכנית וגוזלת זמן.
המעבר של AF לצורה קבועה אינו רצוי מכיוון שהוא מוביל לירידה באיכות החיים, התפתחות CHF, נכות וירידה בתוחלת החיים. על פי מחקר פרמינגהם, AF מגביר את הסיכון לשבץ מוחי איסכמי פי 5, שהסיכון לכך עולה עם הגיל.
תפקיד שלילי של FP:
חוסר סנכרון של עבודת הפרוזדורים והחדרים,
ב/ קרדיומיופתיה הנגרמת על ידי טכיקרדיה,
ג/ סיכון לפתח הפרעות קצב מסכנות חיים,
שלושה גורמים יכולים להשפיע לרעה על ההמודינמיקה: אובדן פעילות מכנית פרוזדורית סינכרונית, התכווצויות חדרים לא סדירות וקצב לב גבוה מדי. ירידה בולטת בתפוקת הלב עקב היעלמות הסיסטולה הפרוזדורית עלולה להתרחש בחולים עם מילוי דיאסטולי לקוי של החדר השמאלי ( היצרות מיטרלי, יתר לחץ דם, קרדיומיופתיה היפרטרופית או מגבילה). העלייה בהפרעות המודינמיות במקרים כאלה יכולה למלא תפקיד קטלני. יש לקחת בחשבון גם את הסיכון לתרומבואמבוליזם סיסטמי חמור. באופן כללי, התמותה ב-AF עולה פי 2. זה נגרם לעתים קרובות על ידי שבץ מוחי, שההסתברות שלו מגיעה ל-5% בשנה, אפילו עם אטיולוגיה לא ראומטית של AF. לפי נתוני מכון המוח בצרפת, 50% מהמקרים המוחיים מתרחשים עקב קרדיואמבוליזם, בעוד שב-40% מהמקרים יש AF קבוע או התקפי, 30% מהחולים הללו מתו במהלך 6 החודשים הבאים (G. Runcural, 1994).
תדירות גבוהה תמידית של התכווצויות פרוזדורים משפיעה לרעה על ההתכווצות שלהם (קרדיומיופתיה פרוזדורית הנגרמת על ידי טכיקרדיה). שינויים אלו עשויים להסביר את ההתאוששות האיטית של התכווצות פרוזדורים לאחר שחזור קצב הסינוס. קצב חדרים גבוה יכול לגרום לקרדיומיופתיה מורחבת. שליטה בתדירות התכווצויות החדרים (שמירה על נורמוזיסטולה) מסוגלת לחסל חלקית או מלאה את התהליכים המובילים לצורה זו של מיופתיה. זה גם מגביר את הסיכון לפתח הפרעות קצב מסכנות חיים, סיבוכים תרומבואמבוליים.
אין ספק שמחקר אינטנסיבי בתחום יצירת AAs חדשים, בעיקר סוג III, יוביל להופעתם של תרופות יעילות ביותר. נתונים שפורסמו לאחרונה על הניסויים של רוסי-גרמני חדש נגד הפרעות קצב מחלקה III AL-275. נכון לעכשיו, נעשה ניסיון לסנתז אמיודרון נטול יוד (דרונדרון), אם כי יש לזכור שתרופה כזו נוצרה פעם תחת השם L-9394 (Woleffie et al., 1973), אך התברר ככזו. לא יעיל, מה שמרמז על מנגנונים אינטימיים של האפקט האנטי-אריתמי.אמיודרון הקשור להשתתפות בהפרעות קצב של הורמוני בלוטת התריס (?).
לפי פרופסור H. Wellens (1997), אפילו במילניום החדש, רופאי קצב יצטרכו לפתור בעיות כמו פרפור פרוזדורים, מספר הולך וגדל של הפרעות בשאיבה של הלב בחולים עם הפרעות קצב, מחוץ לבית החולים. מוות פתאומי. במקביל, הם עזרה תגיעהפרעת קצב מולקולרית וגנטית.
- Smetnev AS, Grossu AA., Shevchenko NM., אבחון וטיפול בהפרעות קצב לב., Chisinau, 1990. אבחון וטיפול בפרפור פרוזדורים, VNOK
- Zamotaev IP, Lozinsky LG, Kerimova RE, נופים מודרנייםעל הפתוגנזה, הפרוגנוזה והטיפול בפרפור פרוזדורים התקפי., קרדיולוגיה, 1990, 5,.
- Antonchenko I.V., Popov S.V., Savenkova G.M. // גירוי לב-98. תקצירים של דוחות. SPb. עלון אריתמולוגיה. 1998. N8. עמ' 53.
לשצ'ינסקי L.A., Tyulkina E.E. טיפול תרופתי בפרפור פרוזדורים. בספר. Egorov D.F., Leshchinsky L.A., Nedostup A.V., Tyulkina E.E. "פרפור פרוזדורים: אסטרטגיה וטקטיקה של טיפול על סף המאה ה-XXI". SPb. איזבסק. מ' 1998. ש' 15-82.